

文章标题:Sub-nanoliter metabolomics via mass spectrometry to characterize volume-limited samples
发表期刊:nature communications
影响因子:15.7
研究背景
代谢组学是解析疾病机制和发现生物标志物的强大工具,在理解疾病状态、监测治疗效果中发挥着关键作用。然而,传统代谢组学方法(如LC-MS/GC-MS)通常需要毫升级别的样本,即便直流模式的纳升电喷雾直接输注质谱也存在技术短板,这使得许多珍贵或难以获取的样本类型难以开展研究——例如婴幼儿的呼出气冷凝物(Exhaled Breath Condensate, EBC)、间充质基质干细胞等稀有细胞、活检组织、外泌体、骨髓造血干细胞等。微量样本分析的核心挑战在于在极低样本消耗下获取高信息密度的高质量质谱数据,而传统直流电喷雾离子化(DC nanoESI/ESI)与Orbitrap、飞行时间等脉冲式质量分析器耦合时,存在占空比低、样本浪费严重的问题,无法实现珍贵样本的高效利用。
研究结果
01.TENGi质谱法
该研究采用TENGi nanoESI离子源(图1a),其核心为滑动独立层式摩擦纳米发电机(TENG)(图1b)。TENG以尼龙层与氟化乙烯丙烯共聚物(FEP)固定层为摩擦对,搭配铜膜电极,通过相对滑动起电,一极接离子源、一极接地。样品置于纳升喷雾发射器内,外部包裹10 mm宽铜箔带作为感应电极,不与样品溶液直接接触,实现非接触式诱导喷雾,既避免交叉污染,又有效消除最小样品体积限制(图1c);发射器经定制卡盒固定,保证尖端与质谱进样口间距恒定。电路上,系统可等效为三电容模型(图1d),其中样品溶液/空气/质谱进样口构成的第三电容为漏电容,当该电容处电荷累积超出溶液承载能力时,液滴发射并启动电离;TENG工作后在二、三电容区域形成强静电场(图1e),通过静电场诱导分子极化、电离与电荷分离触发喷雾电离,无最小进样体积限制,电离高效稳定。
TENGi nanoESI为脉冲式离子化,单脉冲仅消耗皮升级样品。0.8 μL样品在正离子模式下25 min内可产生超1200个信号脉冲,实验后仍剩余约0.6 μL(图1f),既可获取微量样品的高等级质谱信息,又便于稀有样品后续实验。其脉冲特性与Orbitrap、飞行时间质谱等脉冲式分析器高度匹配。总之,与传统直流(DC)ESI/nanoESI持续进样、在分析器扫描间隙大量浪费样品不同,TENGi可同步电离与分析器工作周期,充分利用每一次喷雾事件,显著降低样品损耗(图1g)。
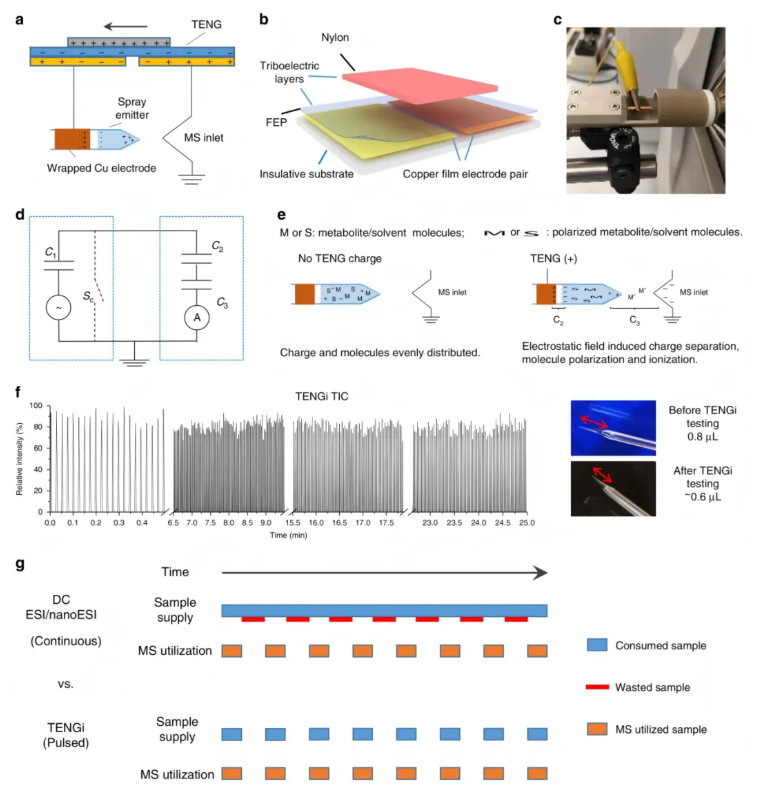
图1.TENG nanoESI的示意图、机理和特性
该TENG具有优良电学性能,最大开路电荷输出1.37 μC(图2a),外接负载实测输出电压可达±5 kV(图2b-c),实际开路输出电压更高;COMSOL模拟显示其开路电压可达数十至数百千伏。传统DC nanoESI因持续高压易发生放电,难以实现该量级的高电压,而TENG的高瞬态电压特性使其具备优异的电离能力。对比四种代谢物标准品,TENGi与DC nanoESI形成的电离加合物相似,但TENGi离子丰度更高(图2d-e),可检出DC nanoESI无法识别的低丰度离子(图2f),且无明显源内裂解。负离子模式下检测EBC中乳酸时,TENGi优势显著(图2g-i):离子丰度为DC nanoESI的5倍,信噪比提升超20倍;DC nanoESI需扫描100次以上,才能达到TENGi单次实验信噪比的1/3(图2i)。综上,TENGi的高灵敏度源于其高电压与有限电荷量的特点。
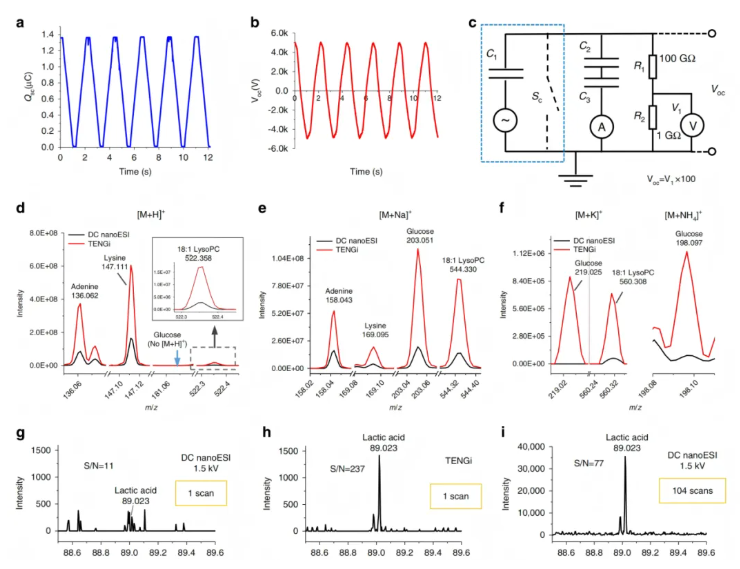
图2.TENG装置和TENGi nanoESI的特性表征
为比较TENGi与传统DC nanoESI在复杂生物样本分析中的覆盖范围,两种技术被用于分析25 μg・mL⁻¹ 稀释肝脏脂质提取物(图 3)。正、负离子全扫描质谱中(图 3a, 3e),TENGi 离子丰度远高于 DC nanoESI;两者均能检测高丰度物质,但 DC nanoESI 无法检测低丰度离子(图 3b, 3f),而 TENGi 可检测这些物质并开展 MS/MS 实验(图 3c, 3g)。正离子模式下,TENGi 检测到 857 个特征峰,DC nanoESI 仅检测到 518 个,TENGi 比 DC nanoESI 多检测 339 个特征峰(图 3d);负离子模式下,TENGi 检测到 413 个特征峰,DC nanoESI 仅检测到 211 个,TENGi 检测的特征峰数量几乎是 DC nanoESI 的两倍(图 3h)。
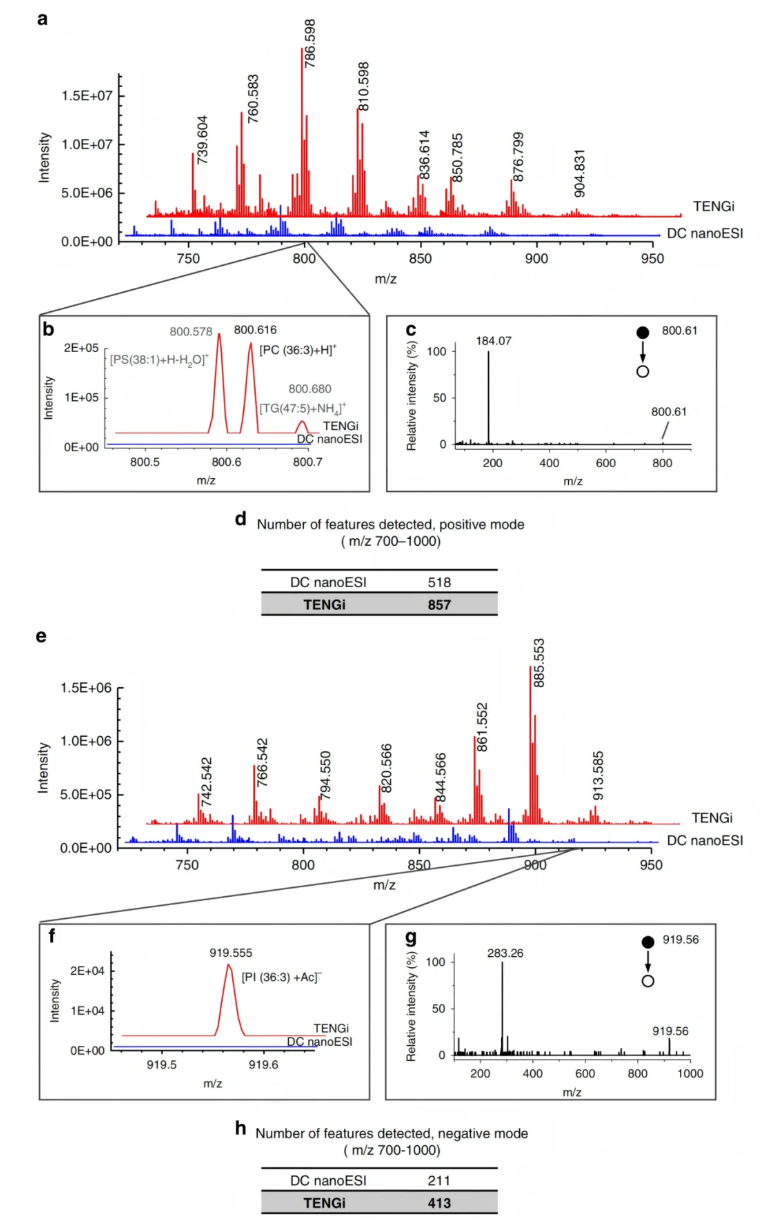
图3.传统DC nanoESI和TENGi MS分析稀释的肝脏脂质提取物
02.囊性纤维化(Cystic Fibrosis, CF)患者的亚纳升代谢组学研究
CF始于婴儿期,监测其婴幼儿呼出气冷凝物(Exhaled Breath Condensate, EBC)代谢表型可助力疾病监测与早期干预。CF相关糖尿病(CF-related diabetes, CFRD)是其常见并发症,会加剧肺功能下降,但相关机制尚不明确。TENGi可实现幼儿EBC微量代谢组学分析,为CFRD早期机制研究提供支撑。
该研究筛选11名CF糖耐量减低(CF prediabetes/impaired glucose tolerance, CF IGT)患者,收集空腹(Pre组)和口服葡萄糖后2小时(Post组)的EBC;因1名患者缺乏Pre组样品、1名患者缺乏Post组样品,最终每组纳入10个样品。TENGi仅需50 μL EBC(收集时间<1分钟)即可完成分析,工作流程如图4a所示。
为保障谱图重现性,采取四项关键措施:(1)使用商用纳升喷雾发射器,保证喷雾尖端直径一致;(2)采用定制卡盒固定发射器(图1c),最大化喷雾位置重现性;(3)通过机械电机标准化TENG的驱动频率与位移距离;(4)添加稳定同位素标记内标,监测每个脉冲的分析质量。实验中QC样品与EBC样品穿插放置(图4b),并通过多步骤数据处理流程(图4c)保障数据质量,具体包括低丰度信号去除、内标归一化、空白信号过滤、缺失值填充与异常样品剔除等。
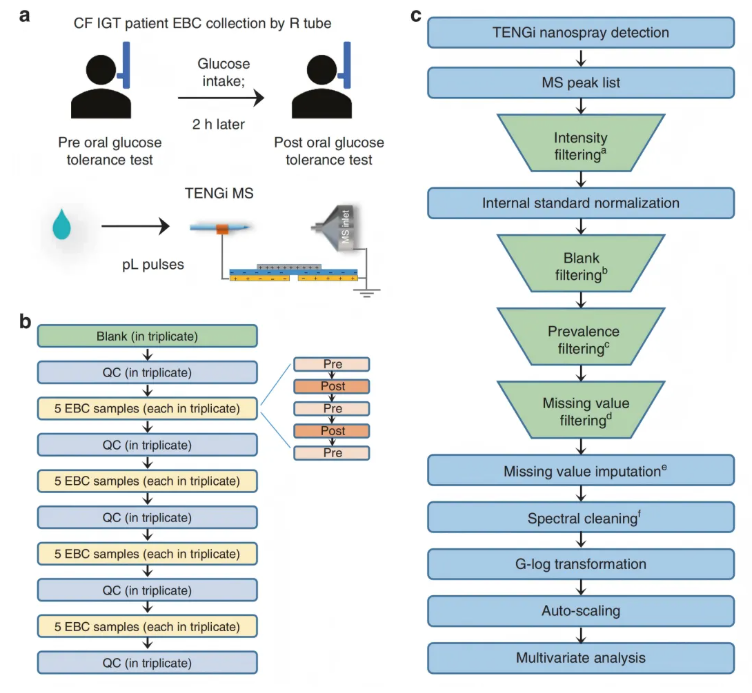
图4.TENGi质谱法分析呼出气冷凝物的实验及数据处理流程
以¹³C标记酪氨酸为内标,监测每个脉冲的内标提取离子流图面积,剔除面积超出预期中位数相对标准差(RSD)±20%的异常脉冲。重现性验证显示,同一发射器与不同发射器的QC样品相对标准偏差(RSDQC)分别为12.8%和17.2%(图5),符合美国食品药品监督管理局(FDA)生物标志物研究的指南要求。
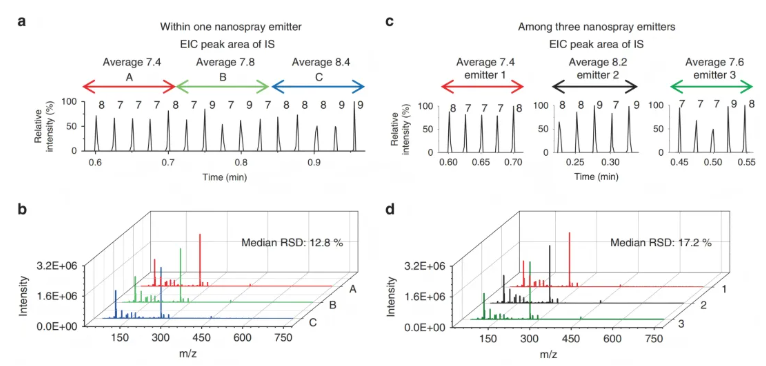
图5.摩擦电离子源在微量代谢组学研究中的重现性验证
多变量分析显示,Pre组与Post组的偏最小二乘判别分析(PLS-DA)得分图分离良好(图6a)。基于火山图标准(p<0.05,折叠变化FC>2或FC<0.5)与PLS-DA VIP得分>1.8(图6b),筛选出5个最显著的判别特征。仅用这5个特征构建的正交偏最小二乘判别分析(oPLS-DA)分类图,交叉验证灵敏度为89%、特异性为70%;5个代谢物在Post组均显著升高(图6c–g)。
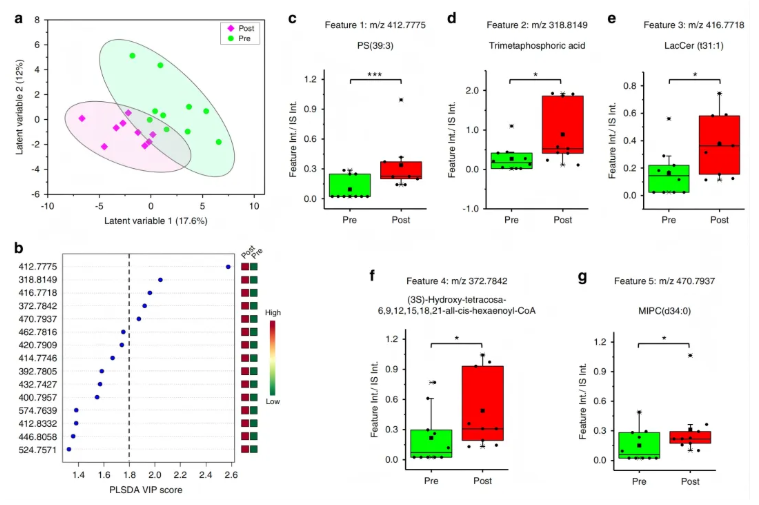
图6.囊性纤维化糖耐量减低患者口服葡萄糖耐量试验前后的TENGi代谢组学分析结果
03.人类间充质干细胞(MSCs)的亚纳升代谢组学研究
基于间充质基质细胞(MSCs)的疗法在骨科、自身免疫性、心血管及神经退行性疾病治疗中前景广阔,其代谢组学研究可解析细胞分化水平、分泌功能、供体差异及疗效评估,为优化疗法关键环节提供支撑。IFN-γ预处理可增强MSCs的免疫抑制能力(如抑制T细胞增殖),解析其在炎症环境下的代谢调控机制对开发改进型MSC疗法至关重要。
该研究仅需80,000个细胞/样品,即可完成代谢组学分析(较传统技术减少20倍细胞用量),对比正常培养与IFN-γ刺激下MSCs的代谢谱差异(图7a)。数据处理流程沿用CF患者EBC样本的策略(图4c),包括低丰度信号去除、内标归一化、空白过滤、缺失值填充等严格步骤。PLS-DA得分图显示IFN-γ刺激组与未刺激组聚类显著(补充图15a),两组代谢谱差异明确。
进一步筛选满足火山图标准(p<0.05,折叠变化FC>2或FC<0.5;图7b)及PLS-DA VIP得分>1.8(图7c)的特征,最终获得14个关键差异代谢物并成功注释,其中1个特征因存在前体离子共选择现象,采用离子迁移谱-质谱(IM-MS/MS)辅助注释。PCA得分图显示两组样本聚类清晰(图7d),载荷图明确了各差异代谢物对分组区分的贡献(图7e);正交偏最小二乘判别分析(oPLS-DA)交叉验证准确率达100%,证实这些差异代谢物与IFN-γ刺激高度相关。
炎症条件下,14个关键代谢物中11个上调、3个下调(图7e):其中次黄嘌呤(ATP分解产物)显著下调,与炎症过程中氧化应激导致的线粒体损伤、ATP耗竭密切相关,符合原文提出的炎症环境下细胞能量代谢紊乱机制。
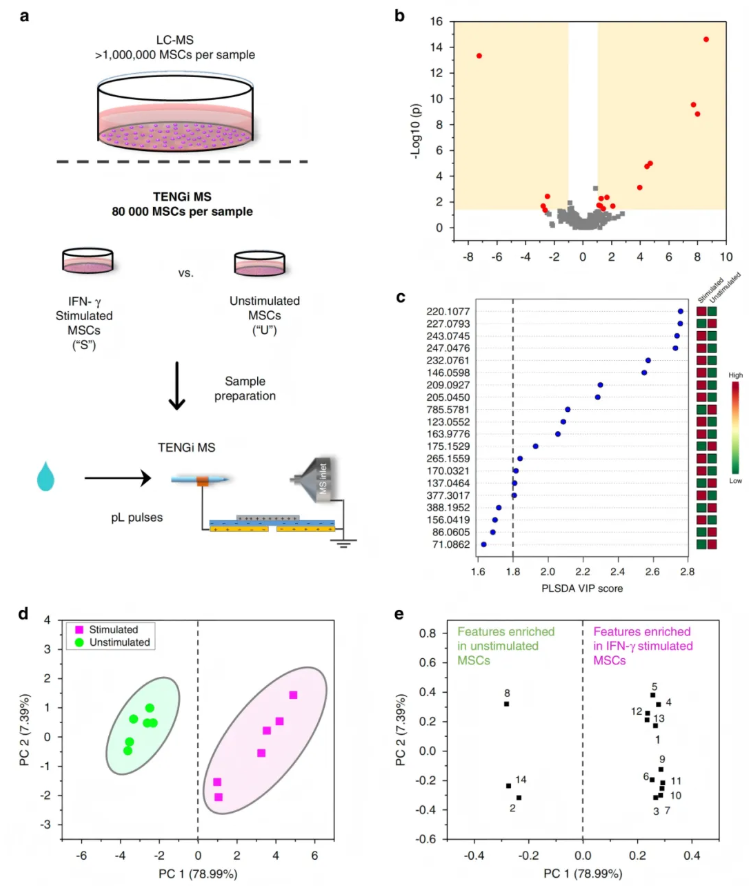
图7.IFN-γ刺激的MSCs的TENGi亚纳升代谢组学研究
热图展示了14个关键代谢特征在每个MSC样本中的表达分布情况(图8a)。通路分析(图8b)显示,色氨酸分解代谢通过三条不同途径发生改变,关键产物包括L-犬尿氨酸、5-羟基-L-色氨酸(5-HTP)和 3-甲基二氧吲哚(3-MDI);其中L-色氨酸、L-犬尿氨酸、5-HTP经标准品MS/MS谱图比对验证,3-MDI通过离子迁移谱-串联质谱(IM-MS/MS)完成结构鉴定。通过皮尔逊相关性分析,筛选并识别出与色氨酸相关的代谢特征,色氨酸(m/z 227.0793)与六种物质呈负相关,其中五种为色氨酸分解代谢产物特征峰(图8c):5-HTP(2个离子峰,m/z 220.1077、m/z 243.0745)、L-犬尿氨酸(2个离子峰,m/z 209.0927、m/z 247.0476)和 3-甲基二氧吲哚(3-MDI,m/z 146.0598),且这五个特征峰的绝对相关系数均>0.8(图8d)。因此,本研究进一步证实IFN-γ刺激可通过三条不同的代谢途径调控MSC的色氨酸分解代谢。
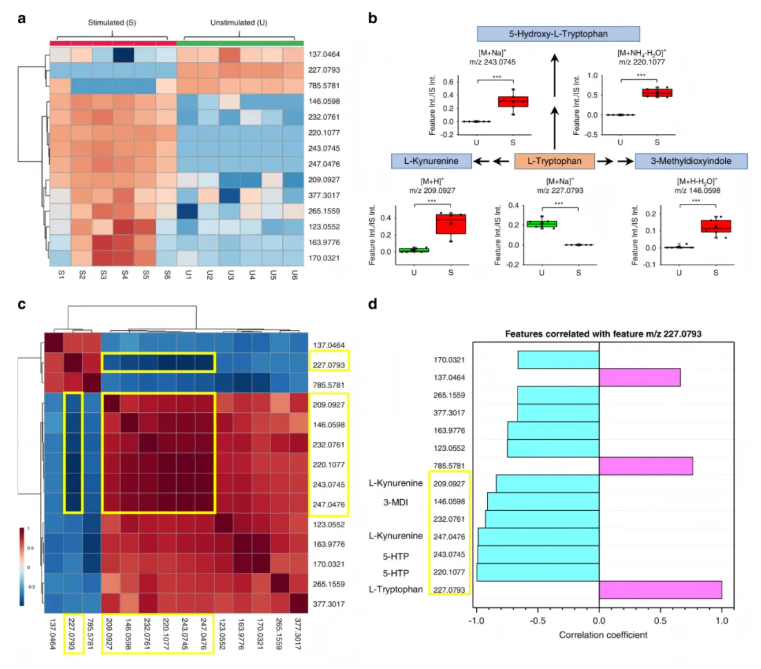
图8.IFN-γ刺激通过三条分解代谢途径影响MSCs中的色氨酸代谢
04.极性切换实验
由于TENG可交替产生正、负脉冲,将该技术与现代质谱仪的快速极性切换能力相结合,可在一次实验中实现正、负离子质谱(MS)信息的同步检测。这种实验模式无需额外开展实验或消耗更多样品,即可在一次样品上样中同时覆盖碱性和酸性代谢物,从而进一步提高每次实验获得的信息密度。
使用50 μg/mL肝脏脂质提取物进行的概念验证实验如图9所示:仅需亚微升样品上样量和亚纳升样品消耗量,就在同一次运行中同时收集到了负离子谱图(图9c)和正离子谱图(图9d),充分验证了该技术的可行性与优势。
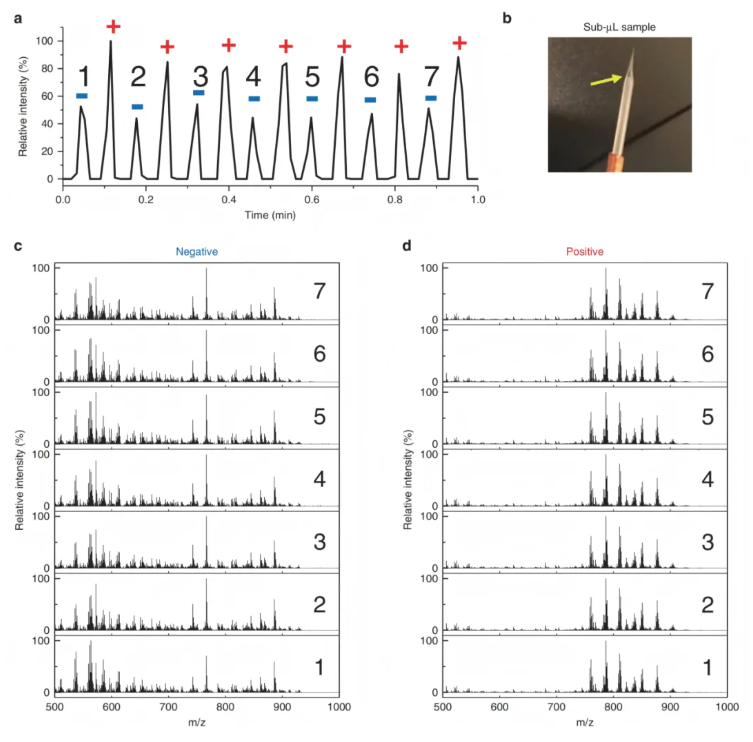
图9.基于TENGi质谱的极性切换技术:亚纳升样品消耗量下一次实验同步采集正负离子信号
研究总结
本研究开发的TENGi-MS技术,成功实现亚纳升级微量样本的代谢组学分析,突破了传统代谢组学对样本量要求较高的技术瓶颈,为微量、珍贵生物样本的代谢研究提供了高效分析工具。该技术在微量样本代谢组学研究中表现突出,针对呼出气冷凝物、间充质基质细胞这类难以获取的微量样本,均能精准识别差异代谢物,还首次发现IFN-γ刺激下,5-HTP和3-MDI两条色氨酸分解代谢通路发生显著变化,丰富了炎症环境下细胞代谢调控的研究认知。这一技术为婴幼儿呼出气冷凝物、稀有细胞等微量样本的代谢组学研究开辟了新途径,也为微量代谢组学技术的发展与应用提供了重要参考。









