产品介绍
普通代谢组学可以反映机体代谢物的变化及可能被激活的通路,同一代谢物可能参与多条代谢通路,但其总含量不发生变化。代谢网络是复杂并且动态变化的,而普通代谢组学仅能提供静态的代谢物丰度信息,因此仍存在局限性,代谢流分析(Metabolic Flux Analysis,MFA)技术则可以很好地弥补这一局限。稳定同位素标记的代谢流分析技术更能体现细胞代谢网络的动态变化,反映遗传或环境因素扰动下的代谢重编程规律。通过在培养液中添加特定标记的底物,将13C或15N标记引入生物系统,随着细胞的生长,底物被吸收并代谢生成不同的代谢物,检测样本中被13C或15N标记上的代谢物,就可以反应细胞的代谢过程。
BIOTREE建立了基于LC-MS/MS平台的非靶标代谢流检测分析方法,不局限于特定的代谢通路,可对临床、动、植物样本进行全面地研究代谢流量随时间变化的动态规律,对流经代谢途径的代谢流量进行定量分析,能够很好的解释代谢物在代谢途径中的变化,将代谢组学的研究提升到更高的水平和层次。
Wang, R., Yin, Y., Li, J. et al. Global stable-isotope tracing metabolomics reveals system-wide metabolic alternations in aging Drosophila. Nat Commun 13, 3518 (2022).
技术优势
◉ 准:对齐国际MSI 标准,level 1鉴定准确率高达98.5%
◉ 严:标准的数据库建立流程;超严格6D质控体系
◉ 全:2w+ BiotreeDB 4.0标准品数据库和专属数据库(临床/植物/脂质专业自建数据库)
◉ 多:高检出,level 1平均检出800+
◉ 广:追踪覆盖范围高,能够对上千个代谢物同时进行稳定同位素标记的追踪
◉ 优:仪器高灵敏、高分辨率,性能稳定
样本要求
液体 | 100 μL/sample |
组织 | 100 mg/sample |
类器官 | 100 mg/sample |
细胞 | 1×10⁷ cells/sample |
检测平台

Orbitrap Exploris 120, Thermo
应用方向
◉ 非靶标代谢流分析可以广泛应用于生命科学和医药研究中,包括细胞代谢调控、代谢新通路、疾病代谢机制、药物新靶标发现与确证、药物药效及毒性评价、疾病诊断或预后生物标志物、药物代谢组学、精准用药等领域
◉ 基因工程:提高基因工程菌目标代谢产物;基因改造前后的代谢功能变化
◉ 疾病机理:揭示肿瘤代谢抑制剂个性化治疗机制;疾病发生发展过程早期诊断的标志物
◉ 代谢重编程:炎症性巨噬细胞免疫代谢重编程机制;植物叶绿体代谢重编程机制
案例应用
英文标题:Sarcosine sensitizes lung adenocarcinoma to chemotherapy by dual activation of ferroptosis via PDK4/PDHA1 signaling and NMDAR-mediated iron export
发表期刊:Experimental Hematology & Oncology
影响因子:13.5
研究背景:肺癌是全球癌症相关死亡的主要原因,其中肺腺癌(Lung Adenocarcinoma, LUAD)是非小细胞肺癌中最常见的亚型,尽管治疗手段不断进步,其五年生存率仍不足26%,化疗耐药是导致预后不良的关键因素之一。铁死亡作为一种铁依赖的脂质过氧化程序性细胞死亡方式,因其能克服传统治疗耐药性而成为研究热点。越来越多证据表明,调控铁死亡可增强肿瘤对化疗的敏感性,但如何精准诱导铁死亡并阐明其代谢调控机制仍不明确。肌氨酸作为内源性代谢物,在前列腺癌等肿瘤中与侵袭转移相关,但其在LUAD中的作用未知。本研究通过代谢组学筛选发现肌氨酸显著增强LUAD细胞对铁死亡诱导剂(Ferroptosis Inducers, FINs)的敏感性。结合临床数据与机制研究,证实肌氨酸通过双重机制调控铁死亡。此外,肌氨酸与顺铂联用可协同增强化疗敏感性,且临床样本中高肌氨酸水平与患者预后改善相关。本研究填补了肌氨酸在铁死亡和LUAD中作用的空白,为克服化疗耐药提供了新靶点,其安全性和代谢调控特性使其有望成为铂类化疗的潜在佐剂,具有重要临床转化价值。
研究结果:
1、代谢物文库筛选揭示肌氨酸增强LUAD细胞铁死亡敏感性
为筛选调控铁死亡的关键代谢物,并验证肌氨酸是否通过特定机制增强LUAD细胞对铁死亡的敏感性,研究首先对铁死亡诱导剂RSL3处理的LUAD细胞系(A549和PC9)进行非靶代谢组学分析,发现肌氨酸显著下调等独特代谢特征(图1A-B)。随后在RSL3诱导的铁死亡模型中,利用包含889种人类内源性代谢物的文库进行筛选,确定肌氨酸为RSL3介导铁死亡的强效增强剂(图1C-D)。
细胞毒性实验显示,肌氨酸与铁死亡诱导剂(如RSL3、IKE)联用可显著降低细胞活力,且该协同效应可被铁死亡抑制剂[脂质过氧化清除剂(Ferrostatin-1, Fer-1)、铁螯合剂(Deferoxamine, DFO)]完全消除,但不受凋亡抑制剂(Z-VAD-FMK)或坏死性凋亡抑制剂(Necrosulfonamide)影响,确认肌氨酸促铁死亡作用的特异性(图1E–H)。进一步检测显示,外源性肌氨酸显著增强RSL3诱导的脂质活性氧(Lipid-ROS)生成(图1I)、胞内亚铁离子积累(图1J)和丙二醛(MDA)水平升高(图1K)。透射电镜观察到肌氨酸处理后细胞线粒体嵴消失、体积缩小等铁死亡特征性超微结构改变(图1L)。
综上,肌氨酸通过增强铁依赖的脂质过氧化和线粒体功能紊乱,显著提升LUAD细胞对铁死亡的敏感性。
图1. 代谢物文库筛选揭示肌氨酸与铁死亡相关
2、肌氨酸通过代谢重编程增强铁死亡敏感性
为探究肌氨酸调控铁死亡的机制,首先采用(15)N-肌氨酸同位素追踪代谢流分析,发现肌氨酸在LUAD细胞中极少转化为甘氨酸等下游代谢物(图2A)。使用透析血清(去除小分子物质)培养细胞后,细胞内肌氨酸几乎不可检测,证实其主要来源于培养基血清,而非细胞从头合成。这一结果排除了肌氨酸通过甘氨酸代谢(如谷胱甘肽合成)发挥作用的可能。
进一步通过非靶代谢组学分析发现,肌氨酸处理后,丙酮酸水平显著降低,柠檬酸水平显著升高,差异代谢物显著富集于三羧酸循环(TCA cycle)通路(图2B-C)。Seahorse能量代谢检测显示,肌氨酸诱导细胞外酸化率(Extracellular Acidification Rate, ECAR)降低、耗氧率(Oxygen Consumption Rate, OCR)升高,证实代谢模式从糖酵解向氧化磷酸化转变(图2D)。活性氧(Reactive Oxygen Species, ROS)检测显示,肌氨酸处理组总 ROS 和线粒体 ROS 荧光强度显著增加,提示线粒体电子传递链电子泄漏增加,导致超氧阴离子生成增多(图2E-F)。此外,通过丙酮酸脱氢酶(PDH)活性检测发现,肌氨酸可显著激活PDH,推动代谢通量进入TCA循环。
综上,肌氨酸通过外源补充直接激活PDH,重塑代谢通路为氧化磷酸化模式,增强线粒体ROS爆发并打破氧化还原平衡,从而特异性提升LUAD细胞对铁死亡的敏感性。该效应不依赖于肌氨酸的代谢转化(如代谢为甘氨酸),而是通过调控代谢流实现。
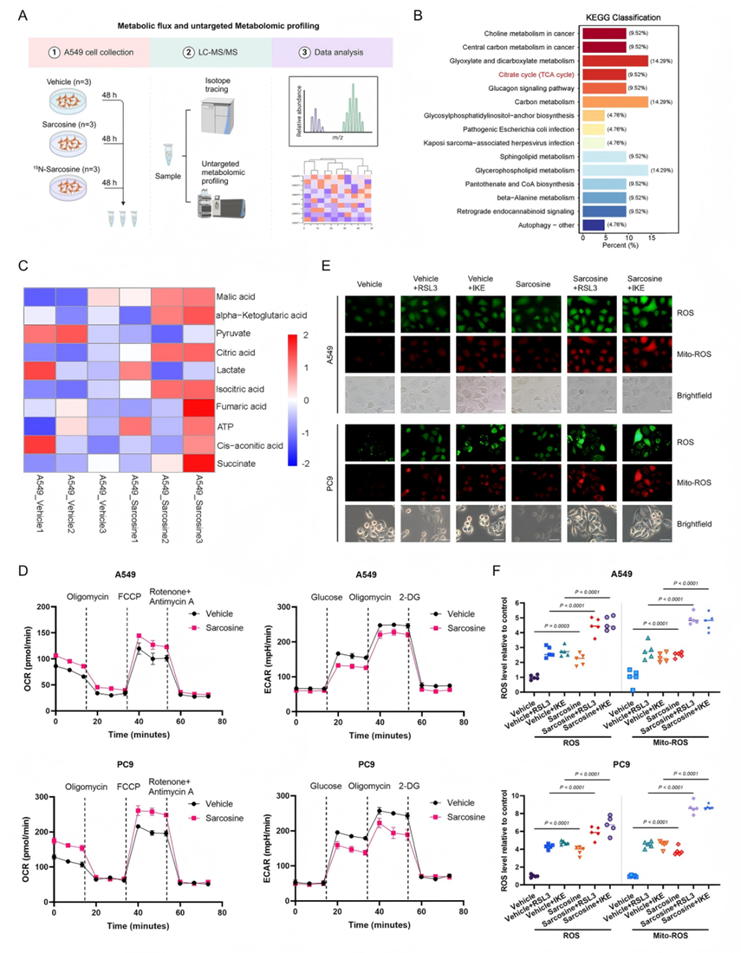
图2. 肌氨酸重塑细胞代谢以增强铁死亡
3、肌氨酸通过抑制PDK4激活三羧酸循环
为探究肌氨酸诱导代谢转向氧化磷酸化并增强铁死亡敏感性的机制,研究发现肌氨酸可显著激活丙酮酸脱氢酶(Pyruvate Dehydrogenase, PDH)活性(图3A),并降低PDHA1(PDH复合物E1α亚基)S293 位点磷酸化水平(图3B)。分子对接实验显示,肌氨酸与PDK4的BCDHK_Adom3结构域特异性结合(图3C)。
通过CRISPR/Cas9技术构建PDK4敲除(PDK4-KO)细胞及BCDHK_Adom3结构域突变体(ΔAdom3,删除 Asp118、Asp182、Ser183),发现PDK4缺失或BCDHK_Adom3结构域突变完全消除了肌氨酸对PDH活性的激活作用(图3D)和PDHA1磷酸化的抑制效应(图3E)。进一步检测显示,PDK4-KO细胞的线粒体ROS(Mito-ROS)水平在肌氨酸处理后显著低于野生型细胞(图3F-G),且对FINs(RSL3/IKE)的敏感性显著增强(图3H-I)。
综上,肌氨酸通过直接结合PDK4的BCDHK_Adom3结构域,抑制其对PDHA1的磷酸化作用,从而激活PDH并推动代谢通量进入三羧酸循环。PDK4抑制是肌氨酸通过代谢重编程增强铁死亡的核心分子机制。
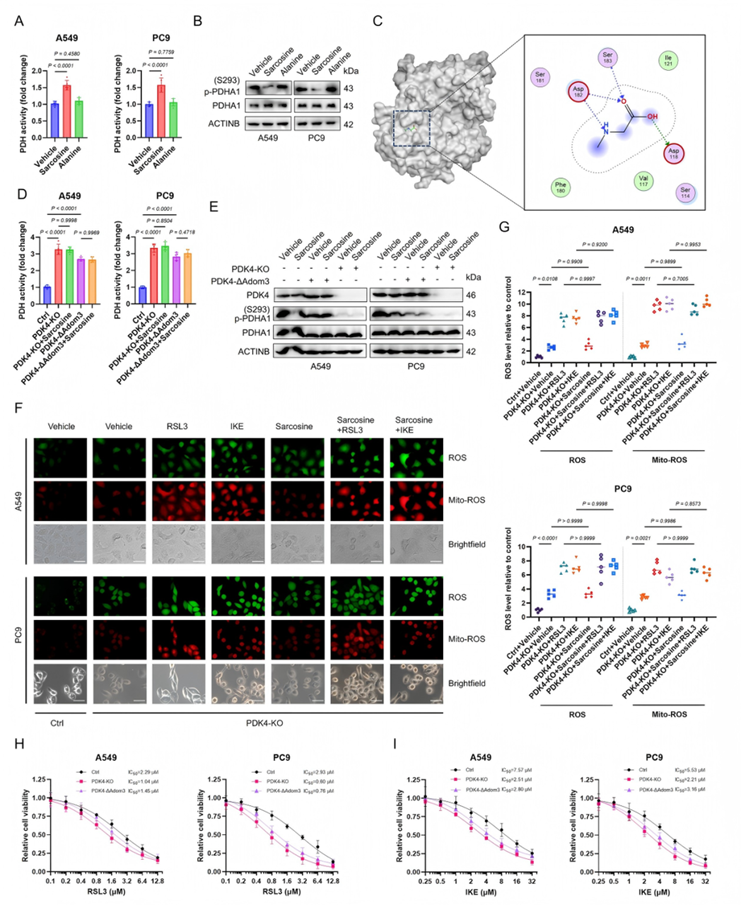
图3. 肌氨酸抑制PDK4,驱动TCA循环激活
4、肌氨酸激活NMDAR/MXD3信号通路以调控SLC40A1
为探究肌氨酸是否通过N-甲基-D-天冬氨酸受体(N-methyl-D-aspartate receptor, NMDAR)信号通路调控铁死亡及其分子机制,研究发现肌氨酸处理显著下调亚铁离子输出跨膜蛋白SLC40A1的表达(图4A)。DEPMAP数据显示,LUAD细胞中SLC40A1表达与肌氨酸丰度呈负相关(图4B)。功能实验表明,肌氨酸可升高细胞内亚铁离子水平(可被DFO逆转),并负调控SLC40A1蛋白表达,而NMDAR拮抗剂MK-801则显著逆转这一效应(图4C-E)。
转录组学分析进一步筛选出HLX、HSF4、MXD3和SCX为差异最显著的转录因子(图4F)。聚焦MXD3发现,其在LUAD中与SLC40A1表达呈负相关(图4G)。构建MXD3敲低/过表达细胞系证实,MXD3缺失可显著上调SLC40A1(图4H-I),而免疫组化显示,LUAD组织中MXD3与SLC40A1表达负相关,与脂质过氧化标志物4-HNE正相关(图4J-K)。ChIP-qPCR证实MXD3直接结合于SLC40A1启动子区域(图4L),荧光素酶报告基因实验进一步显示,MXD3可抑制SLC40A1野生型启动子活性(图4M)。
综上,肌氨酸通过激活NMDAR,诱导MXD3介导的SLC40A1转录抑制,减少铁输出并导致细胞内铁蓄积,从而增强LUAD细胞对铁死亡的敏感性。
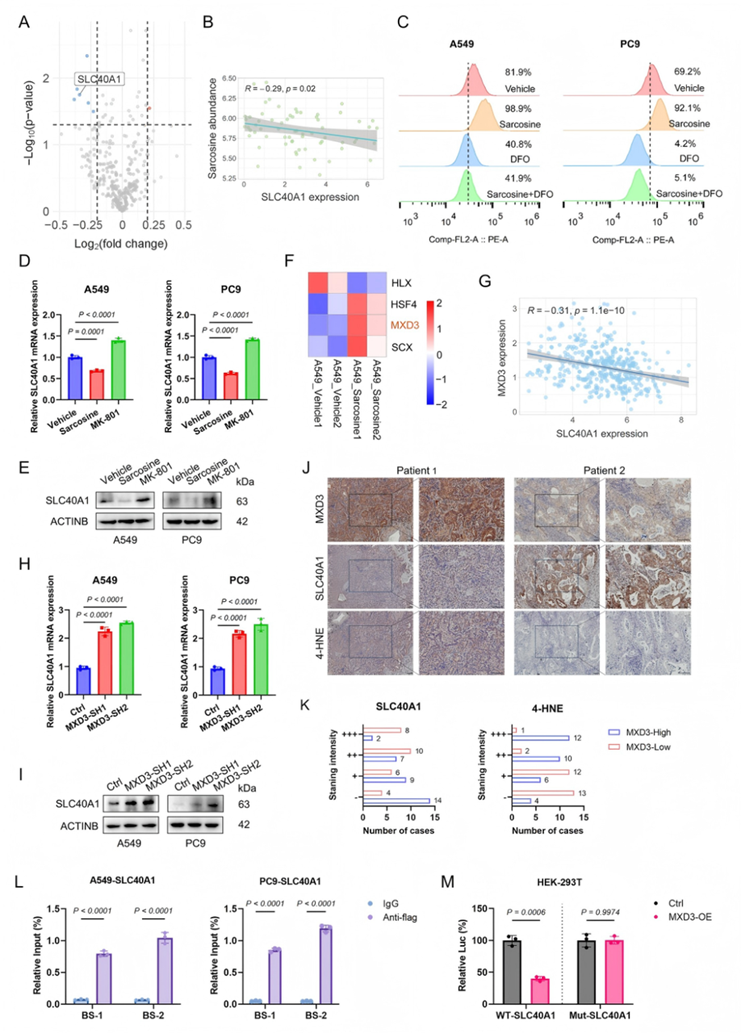
图4. 肌氨酸激活NMDAR/MXD3信号通路以调控SLC40A1
5、PDK4激活和NMDAR阻断逆转肌氨酸介导的铁死亡
为研究PDK4和NMDAR对肌氨酸诱导铁死亡的调节作用,通过构建过表达PDK4的LUAD细胞系(图5A-B)并结合NMDAR药理学抑制实验,发现PDK4异位表达与NMDAR拮抗剂MK-801联用(10 µM),可显著减弱肌氨酸的促铁死亡效应。具体表现为:肌氨酸联合RSL3/IKE诱导的脂质活性氧水平显著降低(图5D),且细胞对铁死亡诱导剂的敏感性降低(图5C)。
综上,PDK4激活与NMDAR阻断可协同逆转肌氨酸介导的铁死亡,揭示两者在肌氨酸调控铁死亡通路中的关键作用(图5C-D)。
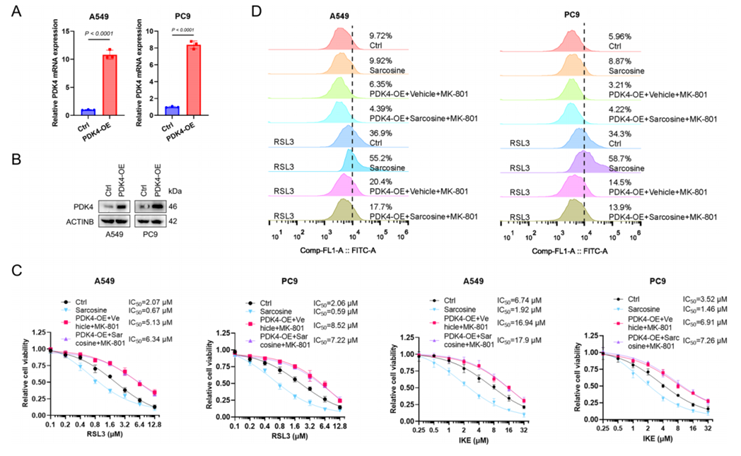
图5. PDK4激活和NMDAR阻断逆转肌氨酸介导的铁死亡
6、肌氨酸通过铁死亡增强CDDP敏感性
为探究肌氨酸是否通过铁死亡途径增强LUAD对顺铂(Cisplatin, CDDP)化疗的敏感性,并验证其临床相关性,研究在LUAD细胞中添加外源性肌氨酸并联合CDDP处理,发现肌氨酸可显著提高细胞对CDDP的敏感性,且该效应能被铁死亡抑制剂(Fer-1、DFO)削弱,证实其依赖铁死亡途径(图6A-C)。单细胞测序分析显示,NMDAR亚基编码基因(GRIN1、GRIN2D)在肿瘤细胞中优先表达,提示肌氨酸作用的肿瘤特异性(图6D-G)。
临床样本分析显示,在120例LUAD患者中,高肌氨酸水平组总生存期(OS)显著优于低肌氨酸水平组(图6H);在41例接受CDDP化疗的亚组中,高肌氨酸水平患者OS呈改善趋势(图6I),且血清肌氨酸水平与OS呈正相关。综上所述,这些数据强调了肌氨酸在增强顺铂疗效和改善LUAD患者预后中的治疗潜力。
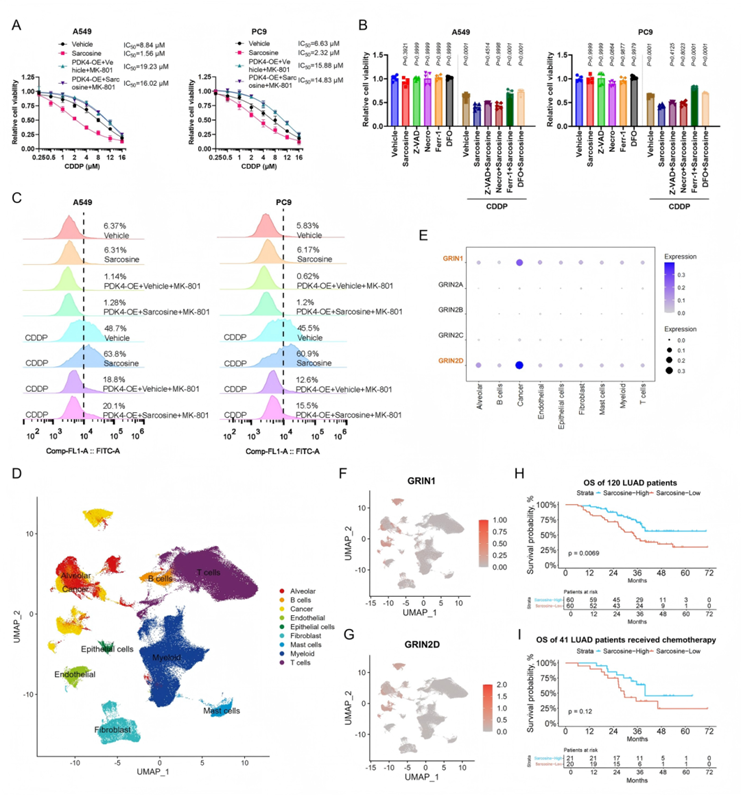
图6. 肌氨酸通过铁死亡增强CDDP的敏感性
7、肌氨酸在患者来源PDOs和异种移植模型中增强治疗效果
为在临床前模型中验证肌氨酸增强铁死亡及化疗敏感性的机制,研究通过慢病毒转染构建PDK4过表达的LUAD类器官(Patient-Derived Organoids, PDOs)模型。形态学观察显示,肌氨酸处理导致PDOs萎缩,ATP酶活性检测证实其代谢活性降低(图7A-B),且对铁死亡诱导剂(FINs)和顺铂(CDDP)的敏感性显著提升(图7C)。NMDAR拮抗剂MK-801处理可显著消除肌氨酸的增敏作用(图7D-E)。
在体内异种移植模型中,对照荷瘤小鼠(Ctrl)接受IKE(40 mg/kg)、CDDP(3 mg/kg)联合肌氨酸(2 mM饮水)治疗时,肿瘤生长显著抑制(图7G-I),而PDK4过表达肿瘤或MK-801处理组中肌氨酸的增强效应消失。多重免疫组织化学(mIHC)分析显示,肌氨酸治疗组肿瘤组织中脂质过氧化标志物4-HNE显著升高,而PDK4过表达或MK-801处理可逆转这一效应(图7J)。
综上,肌氨酸通过依赖PDK4抑制和NMDAR激活的双重机制增强铁死亡和化疗敏感性,在克服LUAD治疗耐药性方面展现出显著治疗潜力。
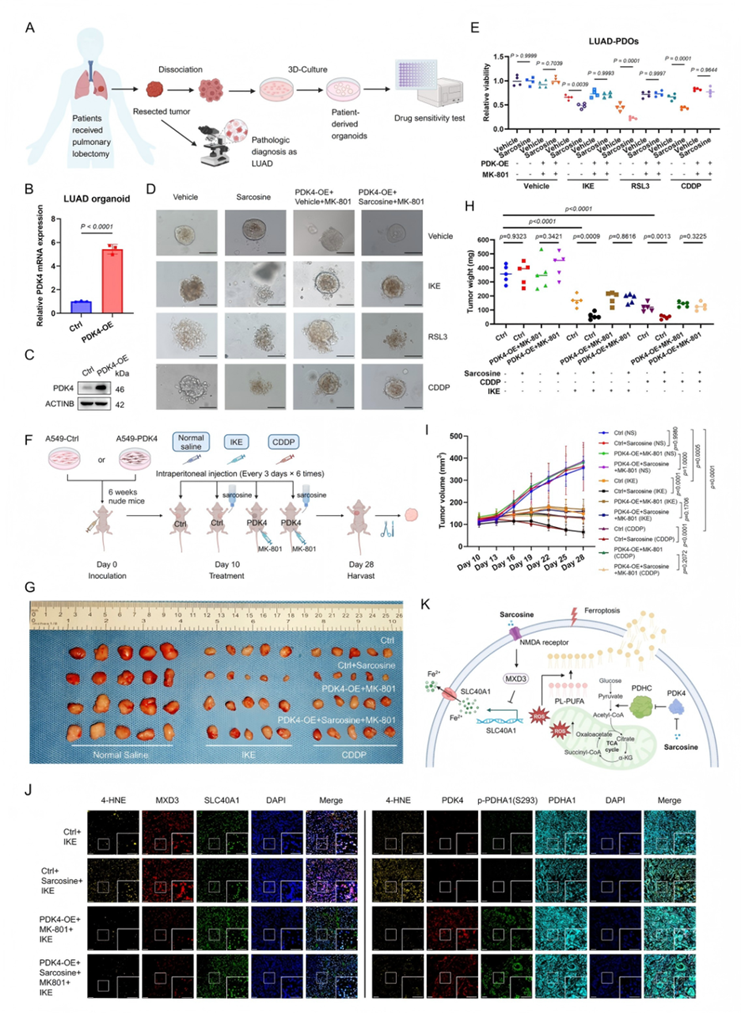
图7. 肌氨酸在患者来源类器官(PDOs)和异种移植模型中增强治疗效果
非靶标代谢流综合解决方案,数据分析软件,质谱检测技术及介绍,全面的联用技术等。








