

文章标题:Amelioration of melittin on adjuvant-induced rheumatoid arthritis: Integrated transcriptome and metabolome
发表期刊:International Journal of Biological Macromolecules
影响因子:8.5
客户单位:云南农业大学、云南中医药大学
百趣提供服务:新一代代谢组学NGM 2 Pro、转录组测序
研究背景
类风湿性关节炎(Rheumatoid arthritis, RA)是一种以侵蚀性、对称性多关节炎为主要临床表现的慢性、全身性自身免疫性疾病,会导致关节僵硬、肿胀、畸形甚至不可逆残疾。该疾病在全球范围内广泛分布,目前缺乏根治方案,且传统药物治疗存在明显副作用。蜂毒肽(Melittin, MLT)作为天然抗炎物质,在RA治疗中展现出显著潜力,但其具体作用机制尚未明确。此前虽有网络药理学研究预测了MLT治疗RA可能涉及的靶点基因(如STAT3、TNF、IL1B等)和信号通路(如TNF信号通路、IL-17信号通路等),但这些预测结果尚未经过体内实验验证,无法明确MLT发挥抗RA作用的具体分子机制。
研究结论
01.MLT对佐剂(Complete Freund’s Adjuvant, CFA)诱导RA的改善作用
关节炎症相关指标改善:治疗周期结束后,MLT和地塞米松(DEX)均显示出治疗效果,有效减轻了CFA注射诱导的病变。二者在改善关节厚度、降低关节炎评分上均达到统计学显著水平,且效果相近;MLT对踝周长的改善效果与DEX相当,但未达到统计学显著水平(图1)。
病理修复:RA疾病模型大鼠与健康对照组相比,足爪表型和组织病理学均呈现显著病变,表现为足爪红肿、关节畸形,严重者甚至蜕皮结痂,病理可见明显的炎症细胞浸润、软骨和骨组织破坏等(图2D)。经地塞米松或蜂毒肽治疗后,D组和M组大鼠足爪红肿缓解、关节结构趋于正常、炎性细胞浸润减少,关节软骨破坏得到部分修复。总体而言,两组治疗均显著恢复了关节结构,涵盖宏观足爪表型和微观关节组织结构(图 A-B)。
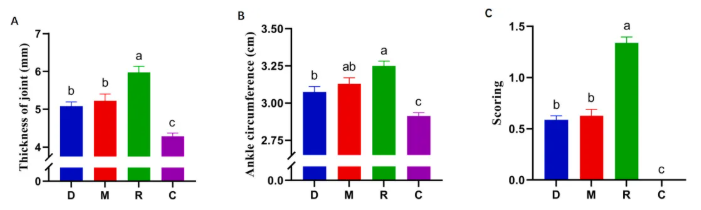
图1. 治疗期结束时大鼠病变关节的炎症指标:(A)关节厚度(B)踝周长(C)关节炎评分
注:D=地塞米松治疗组,M=蜂毒肽治疗组,R=类风湿性关节炎模型组,C=健康对照组
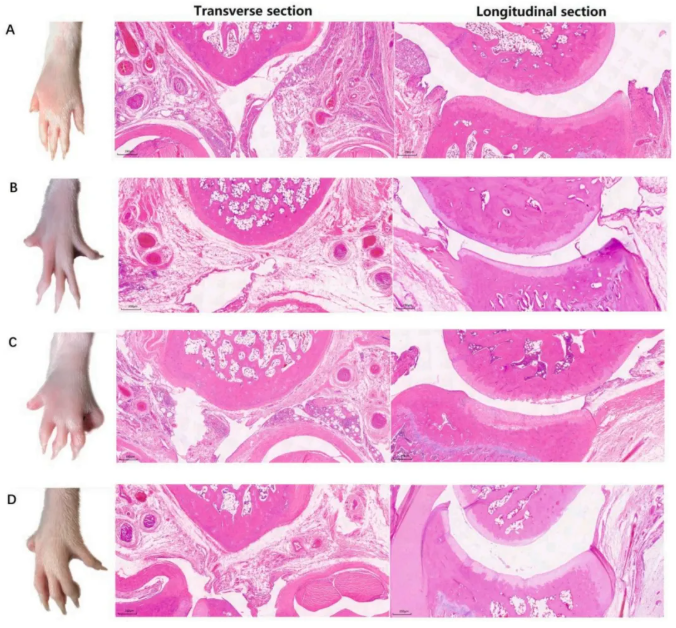
图2. 各组大鼠关节病理切片:(A)地塞米松处理组(B)蜂毒肽处理组(C)RA 模型组(D)正常对照组
02.转录组学分析结果
差异基因:PCA分析结果显示,各组样本间分离良好、组内样本聚集性高(图3A)。与C组相比,R组有2183个DEGs(1687个上调、496个下调),M组有3253个DEGs(2267个上调、986个下调);与R组相比,M组仅21个DEGs(5个上调、16个下调)(图3B-E),提示MLT对RA大鼠的基因表达调控具有特异性和靶向性。
GO富集分析:R组与C组的差异基因主要富集于趋化因子介导信号通路、免疫反应、TNF/IL-1β/IL-6产生等生物学过程;M组与R组差异基因富集于金属离子解毒、锌离子稳态、IL-6受体结合等过程(图4A)。
KEGG富集分析:RA发病相关通路包括细胞因子-细胞因子受体相互作用、MAPK、PI3K-Akt、JAK-STAT、NF-κB信号通路;MLT治疗主要调控细胞因子-细胞因子受体相互作用、TNF、JAK-STAT、HIF-1、FoxO信号通路及类固醇生物合成(图4B-D)。
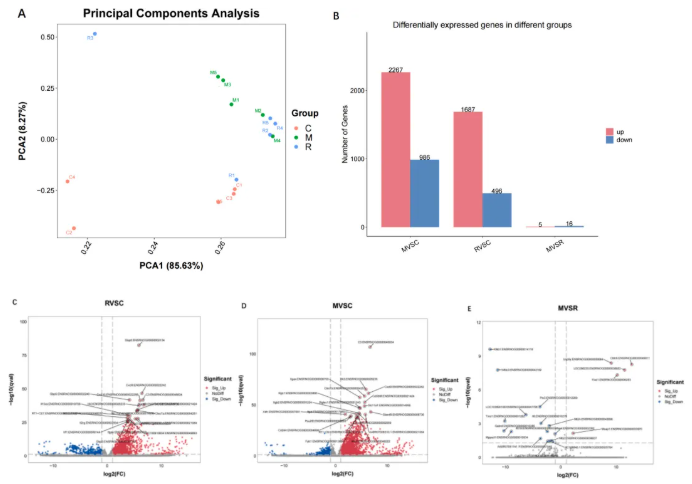
图3. MLT注射对大鼠转录组的影响
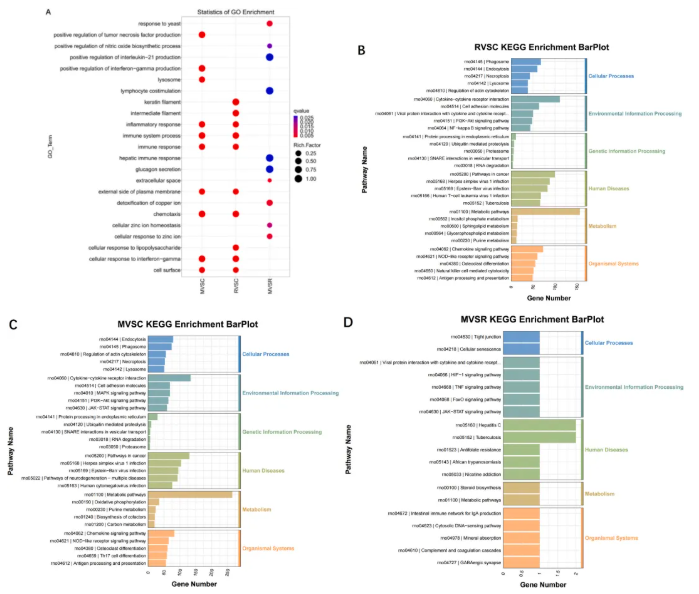
图4. 转录组富集分析
03.代谢组学分析结果
代谢物检测与模型验证:PCA分析显示,M组、C组均与R组呈现明显的分离趋势(图5A);OPLS-DA模型验证可靠,各组间分离效果良好(图5B-D)。
差异代谢物与通路:R组vsC组,差异代谢物主要富集于亚油酸代谢、鞘脂代谢、坏死性凋亡等通路(图7A),关键代谢物包括鞘磷脂(SM(d18:1/16:0))、脂肪酸(顺式-5-十四碳烯酰肉碱)、黄酮类(白杨素-7-O-葡萄糖醛酸苷)(图6D)。M组vsC组,差异代谢物主要富集于癌症中的胆碱代谢、α-亚麻酸代谢、甘油磷脂代谢、花生四烯酸代谢通路(图7B)。M组vsR组,共筛选出421个差异代谢物(图6C、F),MLT可逆转R组中SM、脂肪酸、黄酮类关键代谢物的异常变化,差异代谢物富集通路包括癌症中的胆碱代谢、甘油磷脂代谢,同时还包含鞘脂代谢、坏死性凋亡通路(图7C)。
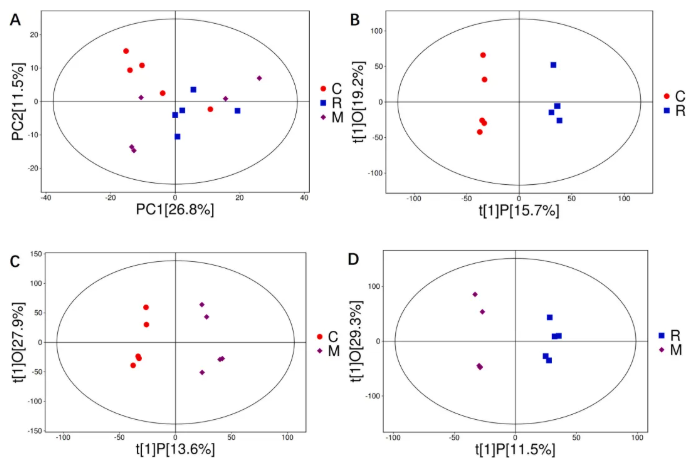
图5. 样本可靠性分析
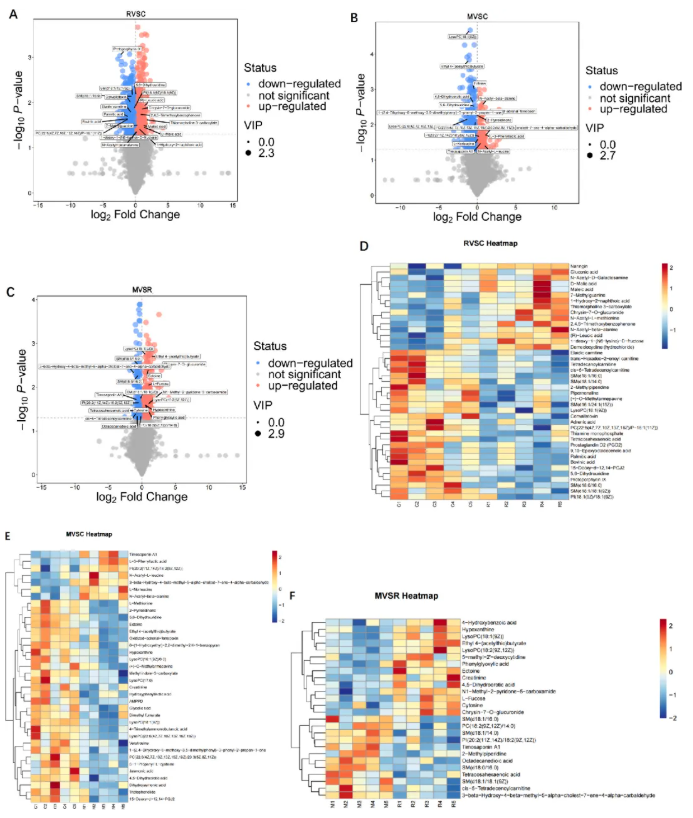
图6. MLT注射对大鼠代谢组的影响
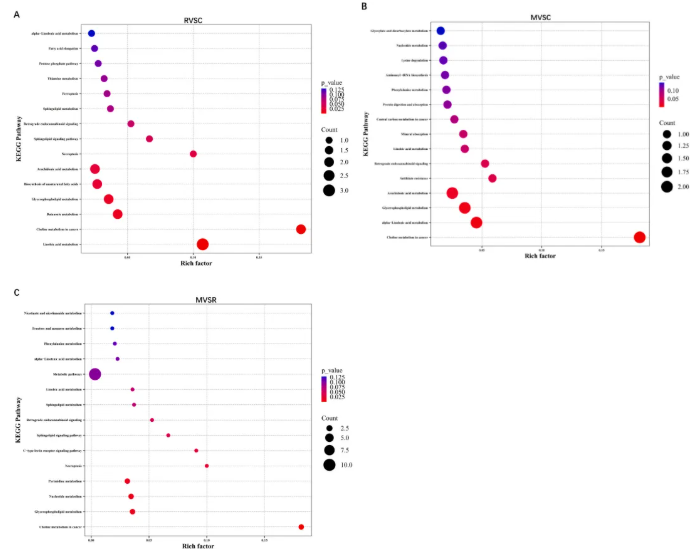
图7. KEGG通路气泡图
04.转录组-代谢组整合分析
相关性与关键通路:鞘脂代谢物与多数差异基因强相关(图8A);共鉴定63条关联通路,包括果糖-甘露糖代谢、嘌呤/嘧啶代谢、IL-17、TNF、JAK-STAT信号通路,其中Il6(Entrez ID:24498)在多个通路中起核心作用(图8B)。
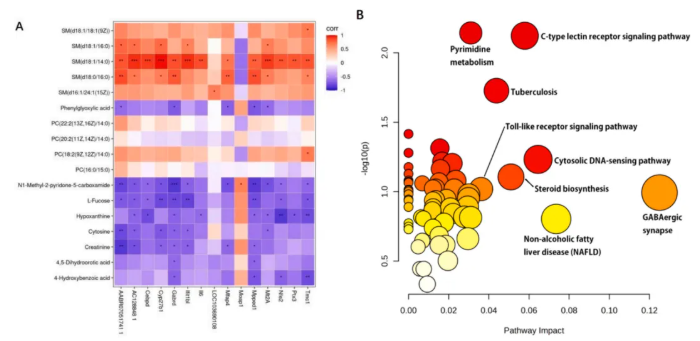
图8. 关键基因与关键差异代谢物的联合分析
05.qRT-PCR与分子对接验证
基因验证:选取12个炎症/抗损伤相关基因(如Il6、Jak2、Stat3、Ptx3),qRT-PCR结果与RNA-seq趋势一致:R组基因上调,M组基因下调(如Il6、Stat3 显著降低)(图9)。
分子对接:MLT与TNF-α(结合能 -10.3 kcal/mol)、IL-1β(结合能 -10.2 kcal/mol)稳定结合,分别形成6个、9个氢键,且存在大量疏水相互作用(图10)。
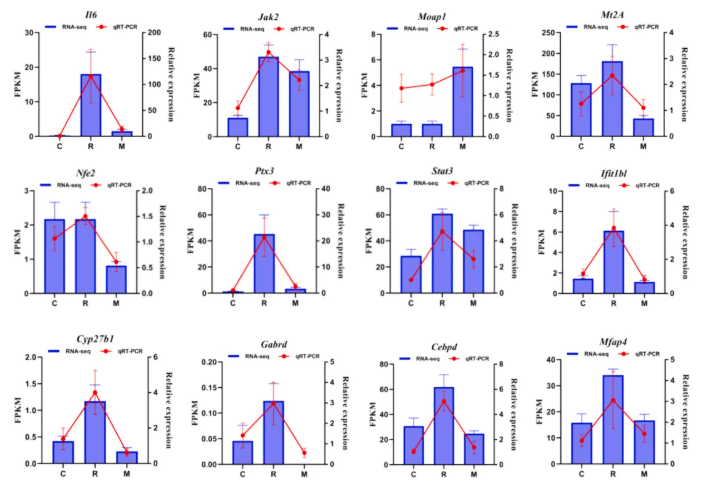
图9. 12个炎症相关基因的转录组测序与qRT-PCR结果
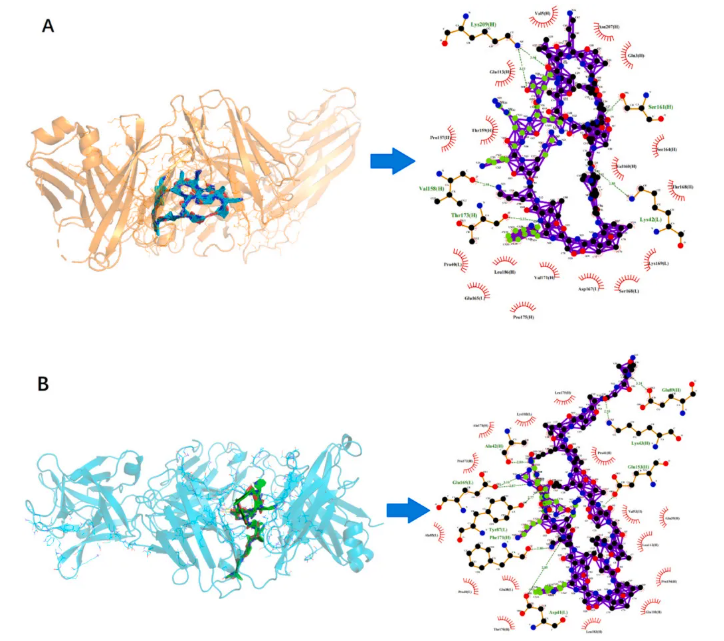
图10. MLT与(A)肿瘤坏死因子-α(TNF-α)、(B)白细胞介素-1β(IL-1β)的分子对接模型(空间结构模型与平面结构模型)
研究总结
该研究证实,MLT对CFA诱导的类风湿关节炎(RA)疗效显著,能有效减轻关节红肿、炎症浸润及骨损伤,效果与地塞米松相当且无激素副作用。其作用机制为:转录层面调控TNF、JAK-STAT等炎症相关信号通路,下调Il6、Jak2等促炎基因;代谢层面逆转鞘磷脂、脂肪酸等标志物异常,改善RA相关代谢紊乱。分子对接显示MLT可与TNF-α、IL-1β稳定结合。研究明确了MLT作为天然抗RA药物的潜力及作用靶点,为其临床应用提供科学依据,未来需通过长期实验完善安全性与作用细节评估。










