
发表期刊:Cell Metabolism
影响因子:31.373
作者单位:复旦大学附属肿瘤医院
发表时间:2022年10月
百趣生物提供服务:非靶代谢组+脂质组检测分析
三阴性乳腺癌(Triple-negative breast cancer ,TNBC)是临床上一种异质性疾病,约占确诊乳腺癌的15%。因异质性高、预后差、复发转移风险高等特点,成为乳腺癌研究中亟需攻克的顽固“堡垒”。2019年邵志敏/江一舟团队根据分子特征、代谢重编程和肿瘤微环境方面的异质性提出三阴乳腺癌的“复旦分型”,随后又针对不同亚型进行了系列精准治疗临床试验。与传统化疗相比,新的疗法治疗效果水平呈上升趋势,但是低于预期。
铁死亡(Ferroptosis)是一种非凋亡性和铁依赖性细胞死亡方式,近年来在肿瘤研究领域表现活跃。在Fe2+或酯氧合酶的作用下,含多不饱和脂肪酸链的磷脂(PE-PUFAs)发生脂质过氧化,诱导细胞铁死亡,这一过程受多种代谢途径的调控,然而TNBC铁死亡的特性仍未揭示。因此TNBC“复旦分型”仍需进一步的研究,探寻新的治疗靶点,以发现TNBC新的治疗突破口。
技术路线
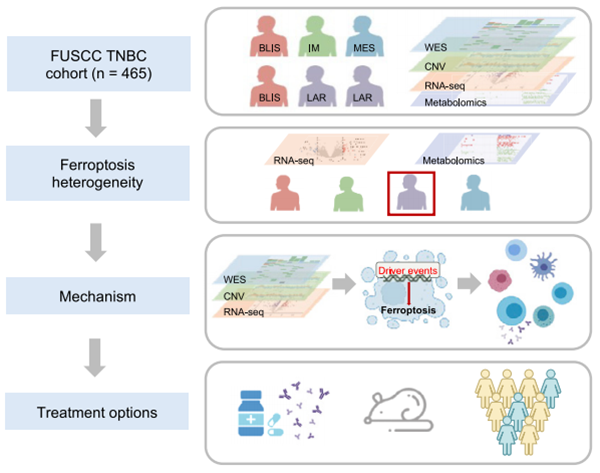
研究结果
1.TNBC“复旦分型”各亚型铁死亡具有异质性
本研究通过对TNBC转录组、非靶代谢组及脂质组数据集分析和验证实验证实“复旦分型”中各亚型铁死亡存在异质性。间质样亚型(Mesenchymal-like, MES)呈现HAMP(铁稳态调节因子,图1C)低表达和铁代谢的失调(图1E);腔面雄激素受体亚型(luminal androgen receptor, LAR)与铁死亡相关的代谢途径被激活(图1A),铁死亡相关基因、蛋白及代谢物出现高度活跃(图1B-F);与LAR亚型相比,免疫调节亚型(immunomodulatory, IM)和基底样免疫抑制亚型(basal-like and immune-suppressed, BLIS)铁死亡相关通路变化水平较低,未出现显著铁死亡相关特性(图1A)。这一结果表明LAR亚型是TNBC中铁死亡敏感性最高的亚型。
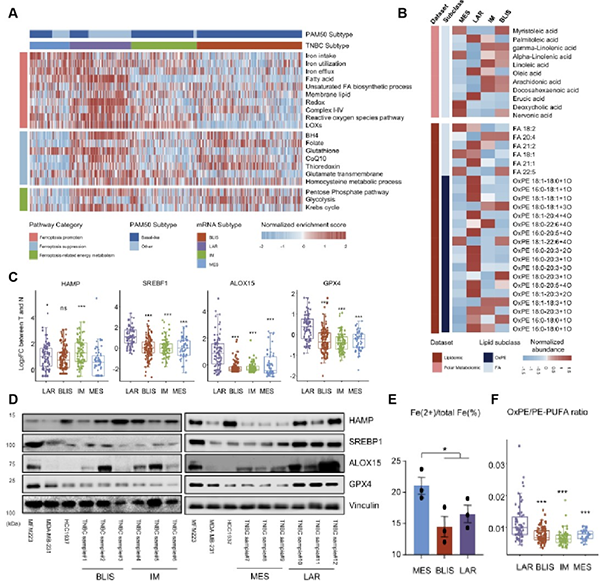
图1. TNBC各亚型中铁死亡相关特征的异质性
2.谷胱甘肽(GSH)代谢中的GPX4是调控LAR亚型肿瘤铁死亡的关键靶点
代谢组通路富集分析显示,LAR亚型肿瘤GSH代谢显著上调,GPX4在LAR亚型肿瘤中表达量高且对铁死亡高度敏感(图1F、图2)。基于以上发现进行细胞和类器官的药敏实验,进一步探索了针对LAR亚型肿瘤铁死亡的最佳治疗策略,结果表明GPX4抑制剂RSL3对LAR亚型抑制效果更加明显(图3)。
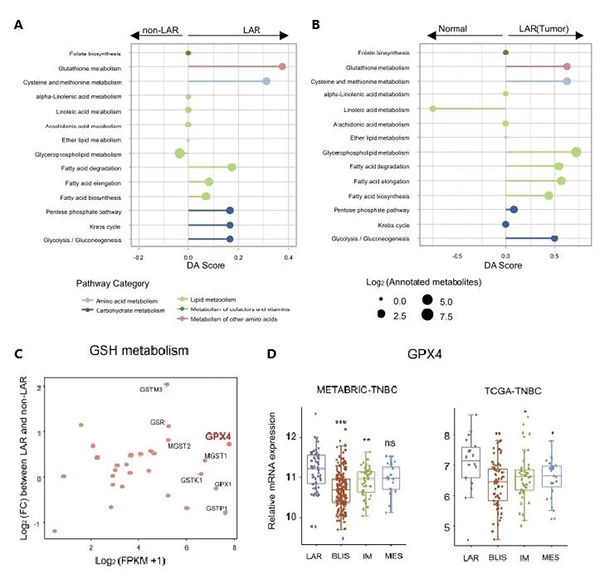
图2. GSH代谢是抑制LAR亚型肿瘤铁死亡的关键
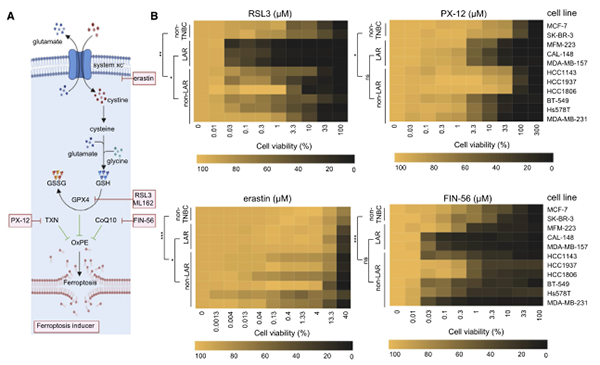
图3. 不同敏感性的铁死亡诱导剂突显了GPX4在LAR亚型肿瘤中的重要性
3. 雄激素受体(AR)与GPX4启动子结合,双向调控LAR亚型肿瘤铁死亡
为了探索LAR亚型肿瘤中GPX4表达增加的机制,作者首先对多组学数据进行分析,结果显示AR信号通路密切相关的FA代谢、雄激素反应等通路与GPX4的表达呈现正相关(图4A)。免疫印迹和qPCR的结果表明,AR对LAR亚型肿瘤中的GPX4起到调控作用(图4B)。进一步的荧光素酶报告基因及ChIP-qPCR发现AR与GPX4-2500~-2000bp启动子区的AR结合位点(AR binding sites, ABSs)结合并驱动GPX4的表达,从而调控LAR亚型中的GPX4高表达(图4C)。
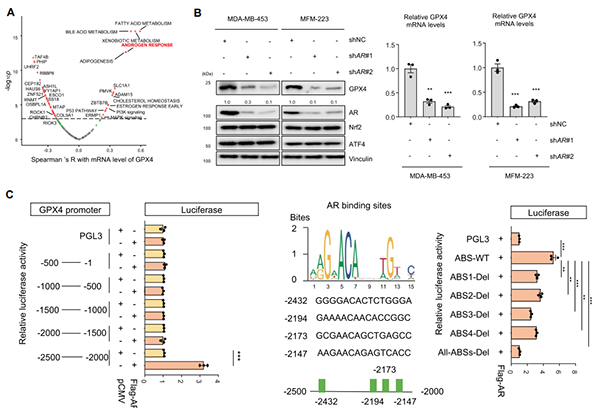
图4. AR是LAR亚型肿瘤中GPX4表达的关键调控因子
基于AR对GPX4的调控作用,作者对AR抑制剂是否与GPX4抑制剂一样,可以作为促进LAR亚型肿瘤铁死亡的潜在抑制因子这一问题进行探究。通过免疫印迹、脂质过氧化检测和BODIPY581/591C11染色对AR抑制剂和GPX4抑制剂诱导的LAR亚型肿瘤细胞系铁死亡进行对比,AR抑制剂并未明显提高肿瘤细胞内脂质过氧化水平(图5A-C),究其原因是AR在细胞中的调控作用是双向的,AR既可以促进铁死亡相关多不饱和脂肪酸的生物合成,又可以上调GPX4的表达,减少引起铁死亡的脂质过氧化(图5D-E)。相较于抑制AR,GPX4抑制剂诱导LAR肿瘤铁死亡的效果更佳。
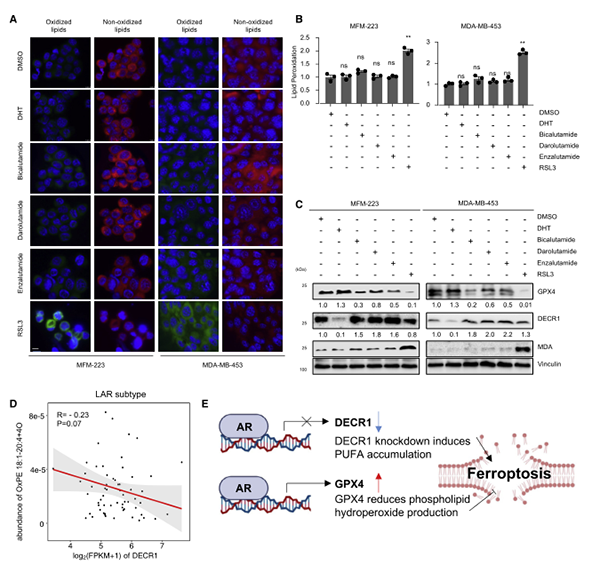
图5. AR具有双重作用来调节铁死亡
4.GPX4抑制剂抑制肿瘤生长、对肿瘤微环境进行重编
基于以上的体外研究,确定了LAR亚型的铁死亡敏感性和GPX4抑制剂具有诱导铁死亡作用。作者通过建立LAR亚型乳腺癌小鼠模型进行体内实验(图6A-B),发现无论是沉默Gpx4基因还是使用GPX4抑制剂都可以显著诱导肿瘤细胞的铁死亡,抑制肿瘤生长,增加CD8+、CD4+等不同亚群T细胞数量,触发肿瘤微环境获得炎症表型,使LAR亚型肿瘤微环境由“冷”转“热”(图6 C-F)。
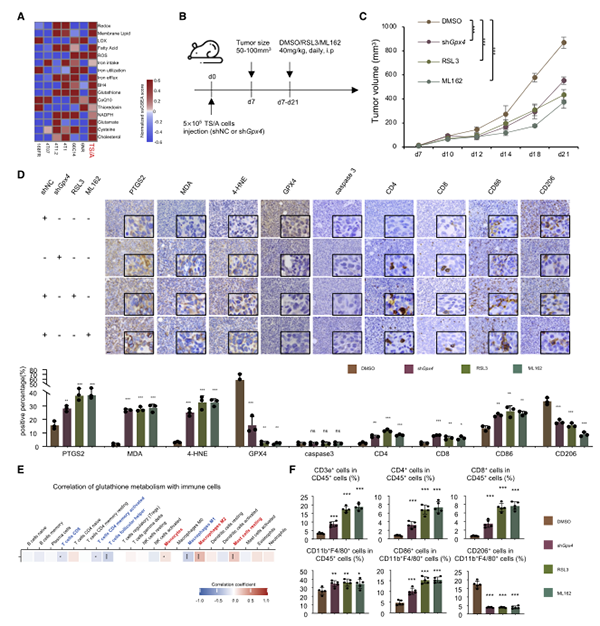
图6. GPX4抑制剂在体内抑制肿瘤生长并重新编程肿瘤微环境
5. GPX4抑制剂联合ICB疗法为LAR亚型肿瘤治疗带来新方向
为了测试GPX4抑制剂和免疫检查点阻断(immune checkpoint blockade,ICB)治疗是否起到协同作用,通过TS/A小鼠乳腺癌细胞系来建立TS/A异种移植瘤进行体内实验(图7A),结果显示与单一治疗相比,GPX4抑制剂和PD-1抗体联合治疗显著抑制肿瘤生长,虽然未引起免疫细胞浸润,但PRF1+CD8+T细胞和GZMB+CD8+T细胞的比例显著增加,出现明显免疫反应(图7)。以上结果表明GPX4抑制剂与ICB联合疗法治疗LAR亚型肿瘤是一种理想的治疗策略,临床免疫治疗及小鼠细胞系免疫治疗队列研究也证实这一结果。
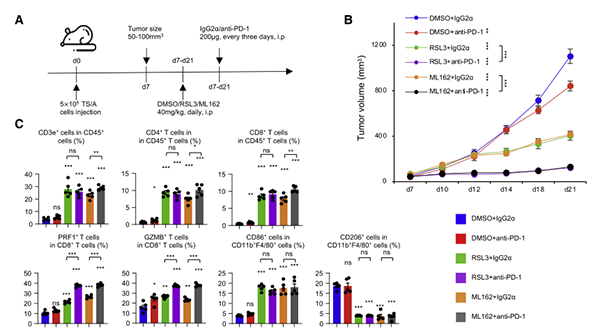
图7. GPX4抑制剂与ICB联用疗法对LAR亚型肿瘤有显著治疗效果
结论
本研究通过多组学数据集分析和体内外实验验证系统地揭示了TNBC“复旦分型”各亚型具有铁死亡异质性,其中LAR亚型肿瘤细胞ROS积累,FA代谢富集,脂氧合酶过度表达,并操纵GSH代谢防止铁死亡的发生。且LAR亚型肿瘤对铁死亡抑制剂、尤其是GPX4抑制剂敏感,是铁死亡治疗最为敏感的亚型。基于这些特征,靶向铁死亡抑制剂与免疫检查点阻断相结合的疗法,为LAR亚型肿瘤提供了精准治疗新方向,为三阴性乳腺癌患者带来新希望。
文献下载链接:
https://pan.baidu.com/s/1k7frsVJXIiLf9C9jyxRDzw
提取码:0000









