

文章标题:Gastrointestinal Environment Intelligent-Responsive Nanozyme for the Treatment of Multidrug-Resistant Helicobacter pylori Infection
发表期刊:Small
影响因子:12.1
客户单位:陕西科技大学
百趣提供服务:微生物多样性测序
研究背景
幽门螺杆菌作为可耐受胃酸的致病菌,全球人群定植率超50%,是胃炎、消化性溃疡的主要诱因,长期感染还可能引发胃癌,根除它可显著降低胃部疾病发病与复发风险。当前临床一线采用质子泵抑制剂/铋剂联合两种抗生素的三联疗法,但耐药菌株增多导致疗效下降,且大剂量抗生素会破坏肠道菌群稳态、引发副作用,同时无法缓解感染诱发的炎症反应。虽有纳米载体可提升抗生素递送效率,却仍未解决抗炎与菌群保护问题,因此亟需高选择性、无耐药性、兼具抗炎效果的非抗生素治疗方案,为多重耐药幽门螺杆菌感染治疗破局。
研究概览
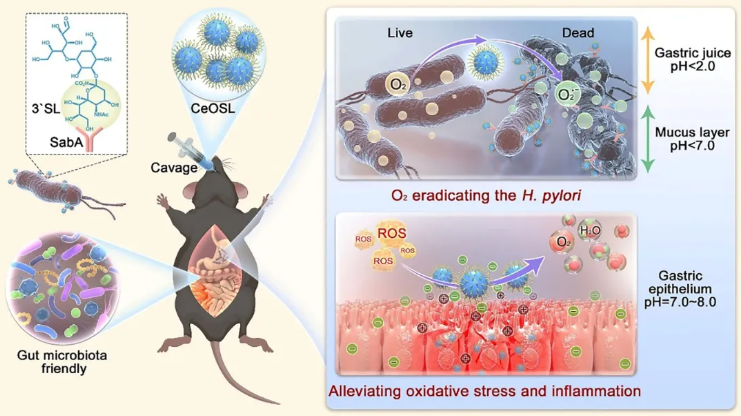
研究结果
01.CeOSL的制备与表征
本研究通过3'-唾液酸乳糖的羧基/羟基与三价铈离子络合,再以2-甲基咪唑调节pH值进行氧化自组装,制得CeOSL(图1a);其透射电子显微镜图像(图1b)显示CeOSL为纳米网状结构,表面分布有大量3'-唾液酸乳糖颗粒,对120个颗粒进行粒径统计分析,确定其平均粒径约2.23 nm,均匀分布于氧化铈表面(图1c)。X射线衍射图谱(图1d)表明CeOSL保持萤石立方相氧化铈晶体结构,衍射峰与标准卡片(JCPDS 34-0394)的(111)(200)(220)(311)晶面对应;因3'-唾液酸乳糖等电点为2.6(pH=7.4时带负电),CeOSL的zeta电位在pH=7.4时为-16.52 mV,pH=3.0时为-9.54 mV(图1e)。X射线光电子能谱(图1f)显示CeOSL的氮元素特征峰显著强于2 nm氧化铈,证实3'-唾液酸乳糖修饰成功;傅里叶变换红外光谱(图1g)中,CeOSL在470 cm⁻¹处有铈-氧-铈键特征峰,3200 cm⁻¹和986 cm⁻¹处分别有羟基、碳氮键特征峰,与 3'-唾液酸乳糖的光谱特征一致;紫外-可见吸收光谱显示其在290 nm处有氧化铈特征吸收峰,且该特征峰在pH=1.0~7.4的磷酸盐缓冲液中保持稳定(图1h)。
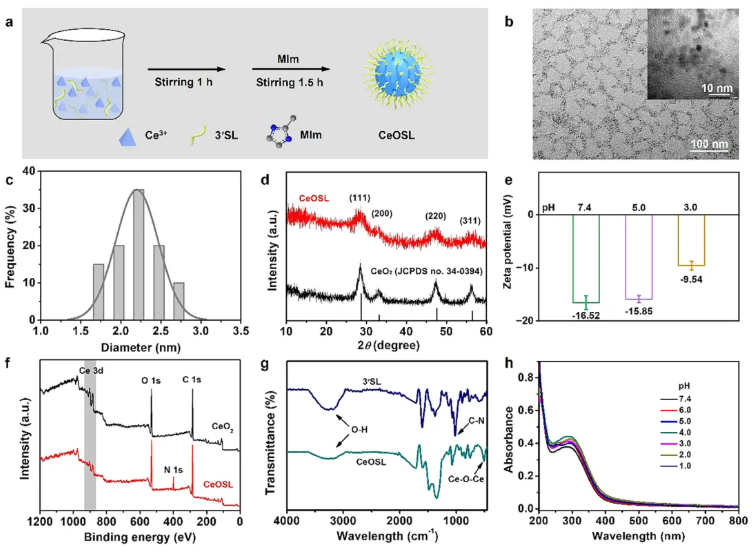
图1.发现队列与验证队列的基线临床特征
02.CeOSL的pH可编程催化特性
本研究以2,2'-联氮双(3-乙基苯并噻唑啉-6-磺酸)(ABTS)为探针,在pH=1.0~7.4(模拟胃液与生理环境)的磷酸盐缓冲液中探究pH对CeOSL催化性能的影响,结果显示随pH从7.4降至1.0,734 nm处特征吸收峰强度逐渐增强,表明其活性氧产生能力具有pH依赖性(图2a-b);以3,3',5,5'-四甲基联苯胺(TMB)为显色剂开展实验,pH>2.0时活性氧将其氧化为蓝色电荷转移复合物,pH≤2.0时被进一步氧化为黄色二亚胺产物(图2c),pH=7.4时溶液无色且无明显吸收峰(图2d),证实酸性条件下CeOSL可催化产生活性氧且产量随pH降低而增加。为明确活性氧种类,用抗坏血酸、二甲基亚砜、超氧化物歧化酶、叠氮化钠分别清除不同活性氧,在pH=4.0时抗坏血酸显著抑制其催化活性(图2e),二甲基亚砜、叠氮化钠对催化活性无影响,超氧化物歧化酶几乎完全抑制氧化反应,证实超氧阴离子自由基是其发挥作用的关键活性物质;X射线光电子能谱分析(图2f)显示,在pH=4.0、1.0条件下催化反应后,CeOSL表面三价铈比例从31.72%分别降至28.74%、26.12%。在生理pH=7.4条件下,CeOSL对超氧阴离子自由基、羟基自由基、过氧化氢三种代表性活性氧的清除能力均具有浓度依赖性(图2g-i)。
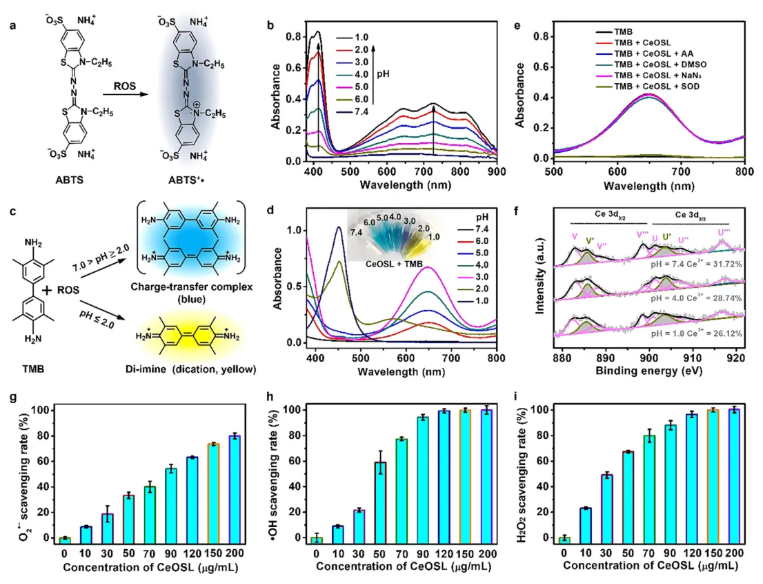
图2.CeOSL的智能响应特性
03.幽门螺杆菌的体外根除实验
在不同pH模拟胃液中,以50 μg/mL CeOSL作用幽门螺杆菌20分钟,琼脂平板菌落计数结果显示(图3a-b):随pH降低菌落数显著减少,pH=7.4时细菌存活率100%(CeOSL类氧化酶活性受抑),pH=5.0~3.0时存活率从45.16%降至0.002%,空腹模拟胃液(pH=1.6)中无存活菌落,证实其可在强酸性环境下产超氧阴离子自由基,通过破坏细菌细胞膜实现强效杀菌。扫描电子显微镜观察(图3c),未加入CeOSL时,幽门螺杆菌在pH=5.0(胃黏液层)、pH=1.6(空腹胃液)的两种模拟胃液中,菌体形态均完整无破损,加入CeOSL后细菌细胞完整性遭到破坏;模拟肠液(pH=7.2)中,CeOSL处理含3,3',5,5'-四甲基联苯胺(TMB)的溶液未出现颜色与光谱变化(图3d,类氧化酶活性受抑),且对粪肠球菌、大肠杆菌无显著抗菌作用(图3e-f),表明CeOSL可在酸性环境中激活类氧化酶活性,实现对幽门螺杆菌的靶向根除,且不损伤肠道菌群。
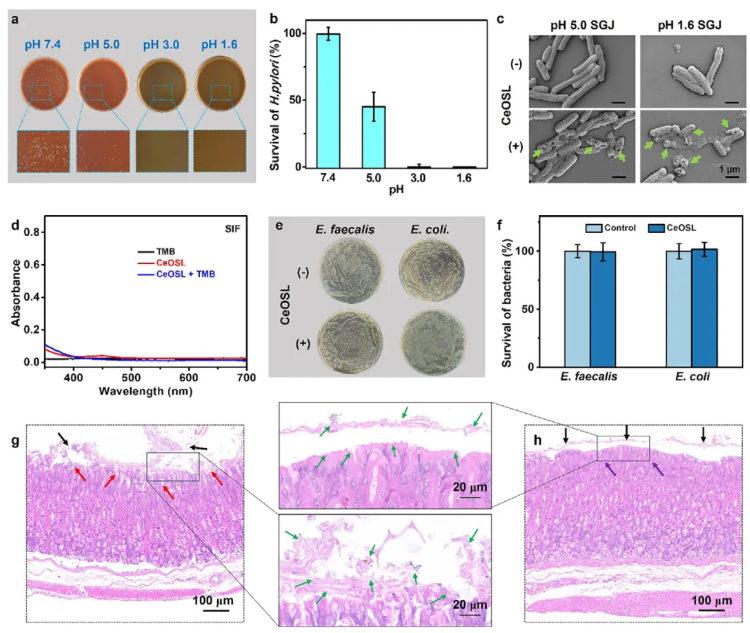
图3.CeOSL体外抗幽门螺杆菌活性测试
04.幽门螺杆菌感染的体内治疗实验
为探究CeOSL的体内生物安全性与抗幽门螺杆菌疗效,对健康BALB/c小鼠灌胃实验显示,每日灌胃2 nm氧化铈或CeOSL连续4天、停药3天后,2 nm氧化铈组胃黏膜层破坏、上皮细胞空泡化(图3g),而CeOSL组胃组织形态正常(图3h),证实其安全性;构建幽门螺杆菌感染小鼠模型(图4a),4周龄小鼠每日灌胃2×10⁸CFU幽门螺杆菌连续4天、饲养2周后,胃组织DNA定量实时聚合酶链反应(qPCR)检测阳性(图4b),将感染小鼠分三组灌胃磷酸盐缓冲液、OAC三联疗法(奥美拉唑+阿莫西林+克拉霉素)或CeOSL连续4天,停药3天后检测,CeOSL组胃内菌落数显著低于OAC组(图4b-d)。HE染色(图4e-f)显示,CeOSL组菌量极少、炎症浸润显著减轻;免疫荧光染色(图5a-d)与酶联免疫吸附实验(图5e-f)证实,CeOSL组促炎因子(白细胞介素-1β、肿瘤坏死因子-α)表达低于OAC组,抗炎因子(白细胞介素-10)表达更高,可在酸性胃液中杀菌、在中性胃上皮细胞中清除活性氧调控炎症。
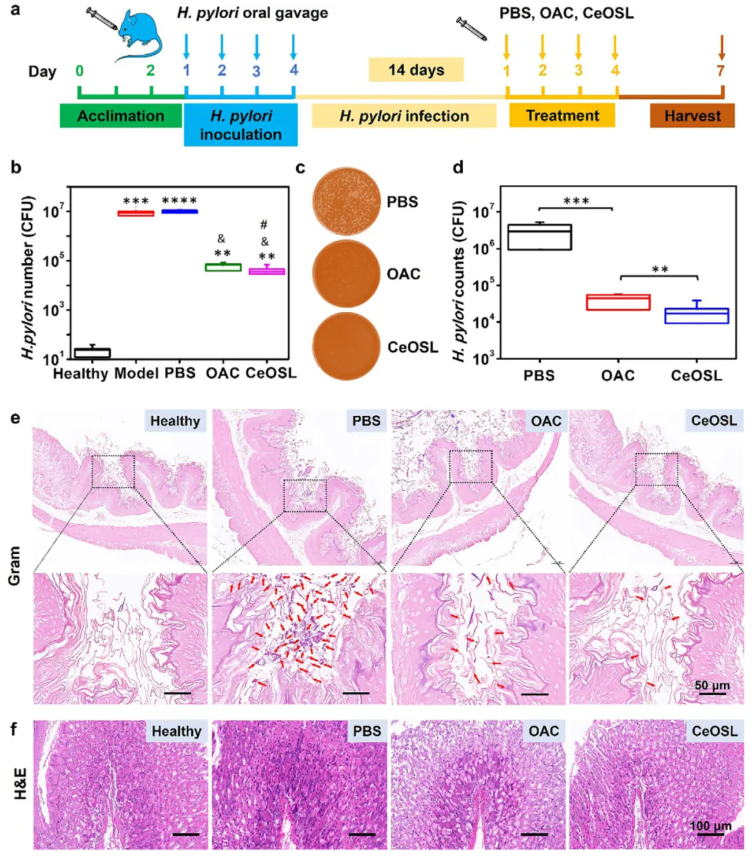
图4.针对幽门螺杆菌感染的体内治疗效果
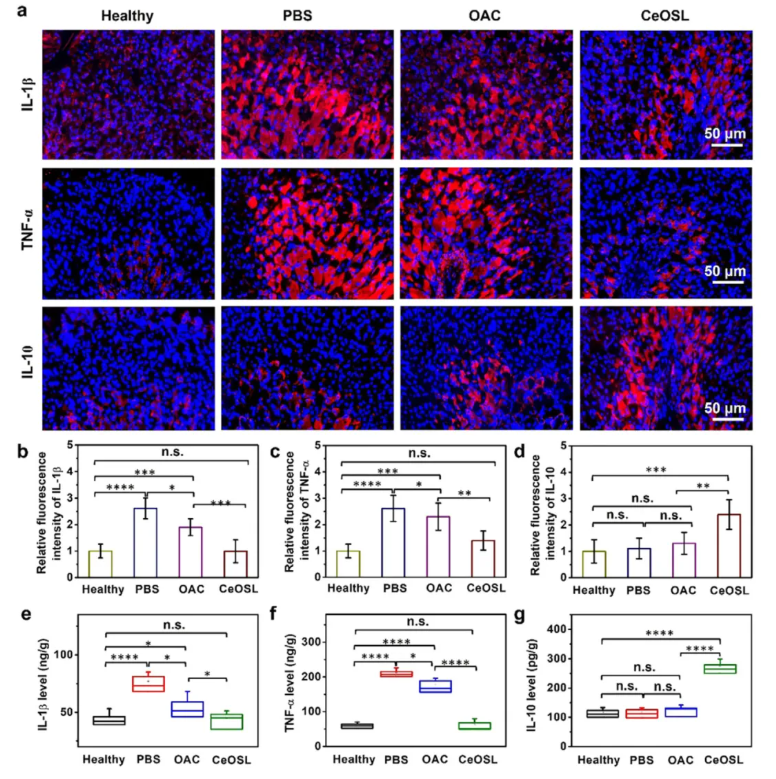
图5.各组小鼠胃组织中 IL-1β、TNF-α 及 IL-10 的免疫荧光染色与 ELISA 检测结果
05.体内肠道菌群分析
采用16S核糖体RNA测序技术分析CeOSL对肠道菌群的影响。α多样性分析显示,CeOSL组的菌群丰富度和多样性显著高于OAC组,更接近健康组(图6a-b)。β多样性非度量多维尺度分析显示(图6c),健康组与CeOSL组的肠道菌群组成相似,且与OAC组存在显著差异。肠道内容物物种丰度热图显示(图6d),健康组和CeOSL组的物种丰度分布相近,而OAC组差异显著。OAC处理后,关键肠道菌群(Lactobacillus、Parabacteroides、Rikenellaceae等)的相对丰度显著低于健康组,而有害细菌(Desulfovibrionaceae、Escherichia、Klebsiella等)丰度显著升高。上述结果表明,CeOSL在中性 pH 条件下通过活性氧清除作用,不会破坏肠道菌群平衡,可避免抗生素类疗法引发的肠道菌群紊乱。
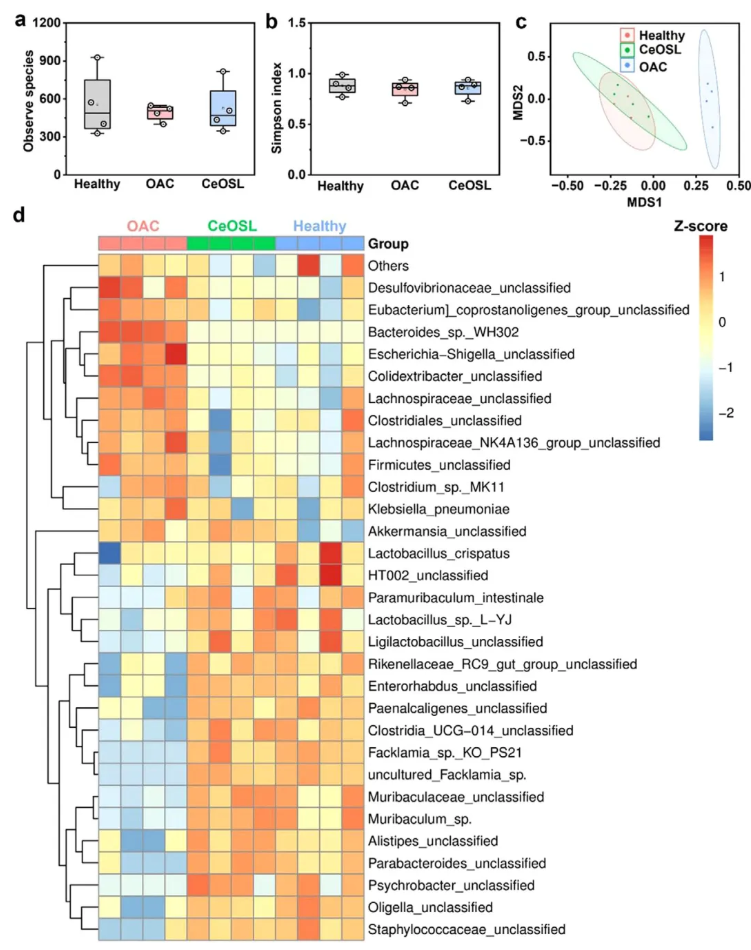
图6.肠道菌群分析
研究总结
本研究研发的胃肠环境智能响应型纳米酶CeOSL,能在不同生理部位选择性根除多重耐药幽门螺杆菌、调节胃上皮炎症并维持肠道菌群平衡:酸性胃液和黏液中激活类氧化酶活性、产超氧阴离子自由基靶向杀菌,中性胃上皮和肠道中类氧化酶活性受抑、转而清除活性氧以缓解炎症。体内实验证实,相较于临床一线OAC三联疗法,CeOSL根除幽门螺杆菌效果更强、减轻胃上皮炎症更有效,且不破坏肠道菌群稳态;其优势在于实现幽门螺杆菌高选择性清除,并借胃肠环境调控纳米酶活性转换同步完成杀菌与抗炎,为幽门螺杆菌相关胃部疾病治疗提供新思路,有望推动高效安全治疗方案研发。









