
文章标题:A skin-hypothalamus axis couples heat stress and metabolic dysfunction
发表期刊:Cell
影响因子:42.5
客户单位:中南大学湘雅医院
百趣提供服务:胶条定性鉴定
研究背景
随着全球气温持续升高,热应激相关慢性健康问题的发病率不断增加。然而,热应激是否对代谢健康产生持久影响尚不清楚。下丘脑作为体温调节和能量稳态的中枢调控器,其星形胶质细胞能够感知环境变化并调节邻近神经元活性,但热应激是否触发星形胶质细胞的表观遗传重编程从而重塑神经元功能仍属未知。
近日,中南大学湘雅医院罗湘杭教授、黄燕副研究员、周海燕教授团队联合山东省立医院赵家军教授团队在线发表题为“A skin-hypothalamus axis couples heat stress and metabolic dysfunction”的研究论文。本研究发现,慢性热应激通过皮肤来源的激肽释放酶相关肽酶14(KLK14),在下丘脑LRRC7⁺星形胶质细胞中建立持久的表观遗传 “热记忆”;这些星形胶质细胞通过ALKBH1介导的N6 mA去甲基化增强GABA合成,抑制PVNOXT神经元活性,进而经交感神经系统(Sympathetic Nervous System, SNS)驱动内脏脂肪沉积,并加剧饮食诱导的代谢功能障碍。在临床队列中,职业性热暴露同样与代谢紊乱显著相关。口服维生素A可降低KLK14水平,在小鼠和人体中均能缓解热应激诱导的代谢损伤,为应对气候变暖带来的代谢健康挑战提供了低成本干预策略。
研究结果
01.热应激暴露加速小鼠和人类的代谢紊乱
急性热暴露可短暂增强能量消耗和胰岛素敏感性,但慢性热应激的长期代谢影响仍不明确。为此,研究将8周龄雄性小鼠随机分为热应激组(Heat Stress, HS)、配对喂养组(Paired-Fed, PF)和室温组(Room Temperature, RT),经2周静息期(Quiescent Stage, QS)恢复后,给予正常饮食(ND)或高脂饮食(HFD)持续10周(图1A)。结果显示,ND条件下HS小鼠的体重与糖稳态无显著变化,仅能量消耗(Energy Expenditure, EE)轻度降低;而HFD喂养后,HS小鼠出现明显代谢紊乱,表现为体重显著增加、糖耐量受损、胰岛素抵抗加重(图1B–D),同时附睾白色脂肪(eWAT)和腹股沟白色脂肪(iWAT)重量上升、脂肪细胞肥大(图1E–F)。
HFD喂养的HS小鼠eWAT中脂解与脂肪酸氧化通路显著受抑,ATGL、p-HSL、TH及PPARα蛋白水平明显降低,iWAT中效应较轻,脂肪合成相关蛋白FASN和SCD1无明显变化(图1G);棕色脂肪(BAT)的脂解与产热标志物无显著差异。在体重尚未出现差异的HFD喂养4周节点,代谢笼检测显示HS小鼠已出现EE降低、呼吸交换率(Respiratory Exchange Ratio, RER)升高(图1H–I),提示脂质利用减少。离体脂解实验显示,eWAT基础甘油释放显著下降,但β3肾上腺素能激动剂CL-316,243诱导的脂解不受影响(图1J–K);同时脂肪组织去甲肾上腺素(NE)水平显著降低(图1L),说明交感神经驱动受损是脂解能力下降的主要原因。上述代谢改变在静息4周、8周后仍可检测到,表明热应激可造成持久的代谢印记。
临床研究以长沙外卖骑手为队列,连续监测夏季热暴露情况,并在3个时间点评估代谢表型(图1M–N)。342名受试者完成全部随访,校正协变量后显示:33°C–36.9°C高温暴露与体重、BMI、腹部内脏脂肪面积(AVFA)长期升高呈正相关;≥37°C极端高温还与腰围、空腹胰岛素及HOMA-IR升高相关(图1O),证实持续性职业热暴露可引发持久的代谢功能障碍。
综上,慢性热应激会损害脂质代谢,导致内脏脂肪过度积累并诱发代谢紊乱。
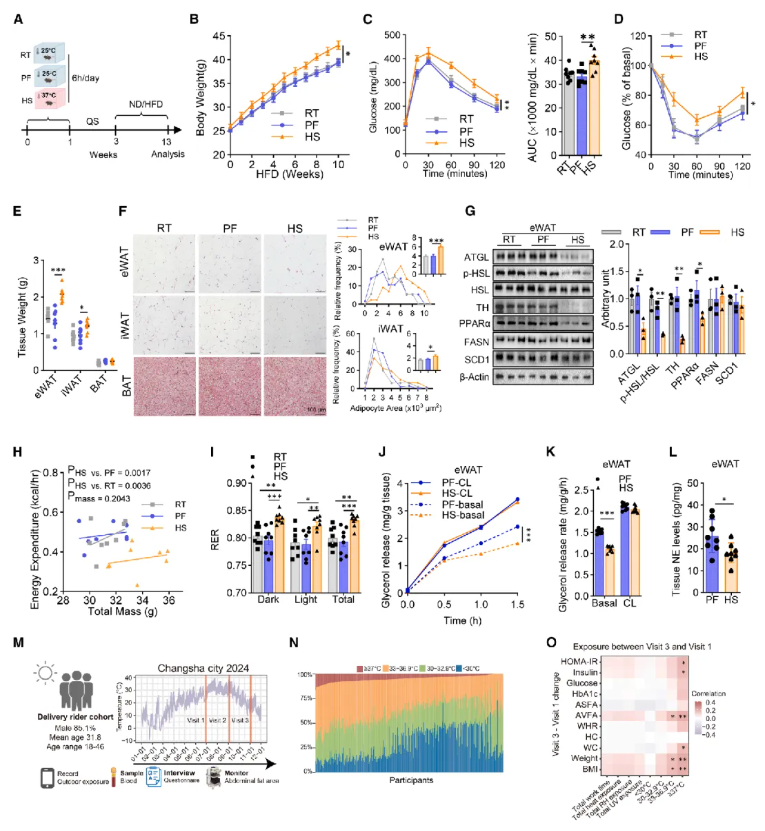
图1.热应激暴露加速小鼠和人类的代谢紊乱
02.下丘脑LRRC7⁺星形胶质细胞在热应激后保留持久热记忆
下丘脑是体温调节与能量稳态的中枢调控器官,其星形胶质细胞可感知环境变化并调控邻近神经元活性,但热应激能否诱导星形胶质细胞形成持久的表观遗传记忆仍不明确。
研究对PF、HS和QS小鼠下丘脑进行单细胞测序(scRNA-seq),发现星形胶质细胞在HS与QS组均显著扩增;聚类分析识别出7个星形胶质细胞亚群,其cluster 2扩增最为显著,其特征标志基因为Lrrc7。基因集变异分析(GSVA)显示,LRRC7⁺星形胶质细胞富集于Ca²⁺信号、细胞黏附及GABA能突触传递通路;流式细胞术证实,该类细胞在HS及后续QS阶段持续增多(图2A–D)。
细胞定位结果表明,HS诱导的LRRC7⁺星形胶质细胞特异性富集于下丘脑室旁核(PVN),而不分布于视交叉上核(SCN)、背内侧下丘脑核(DMH)、腹内侧下丘脑核(VMH)、下丘脑弓状核(ARC)和外侧下丘脑(LH)区域(图2E–F)。
为验证表观遗传热记忆的形成,研究分离LRRC7⁺星形胶质细胞进行染色质可及性测序(ATAC-seq),结果显示3338个热诱导的开放染色质位点可持续维持至静息期,且相关基因富集于GABA能突触与 Ca²⁺信号通路;这些开放染色质区域可稳定保持4周,约8周后逐渐关闭,提示热记忆呈时间依赖性衰减(图2G)。
研究采用二次热暴露范式验证记忆的可召回性:初次热应激小鼠经8周静息后接受二次热刺激(循环热应激,cycHS),与仅接受一次热应激的小鼠(初次热应激,primHS)相比,其LRRC7⁺星形胶质细胞出现显著的表观遗传记忆召回,热记忆特征评分更高(图2H–I)。高脂饮食喂养后,cycHS小鼠表现出更严重的肥胖、糖耐量受损与胰岛素抵抗,同时能量消耗降低、脂质利用减少,而摄食与自主活动量无显著差异(图2J–N)。
以上结果表明,热应激可在 LRRC7⁺星形胶质细胞中形成持久且可召回的表观遗传热记忆,并在致肥环境下加剧代谢紊乱。
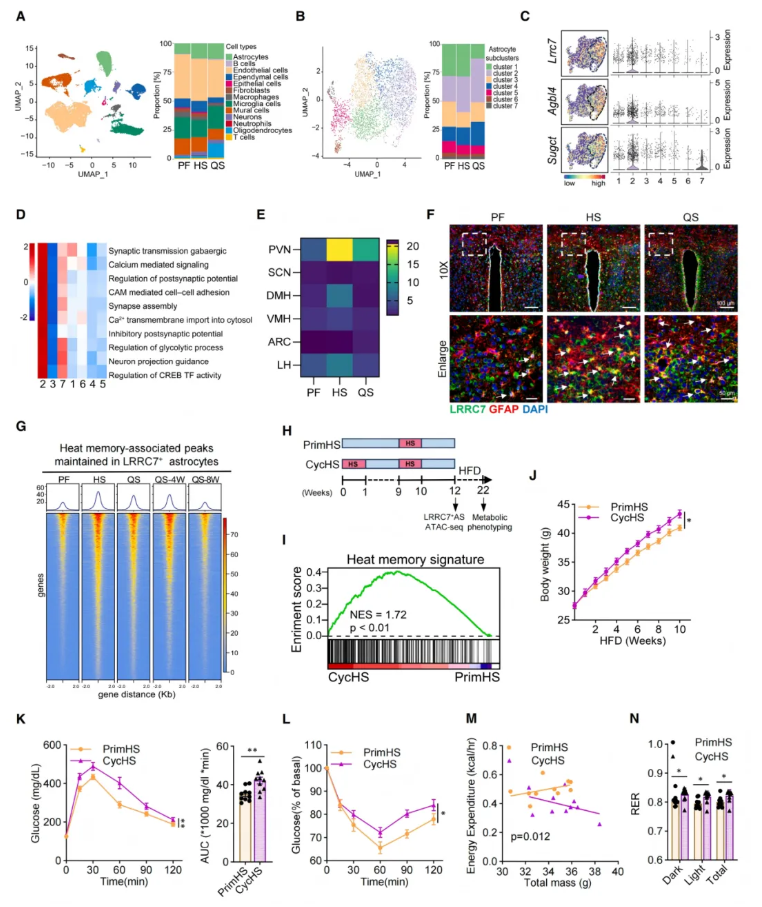
图2.下丘脑LRRC7⁺星形胶质细胞在热应激后保留持久的热记忆
03.LRRC7⁺星形胶质细胞的热记忆使小鼠易患饮食诱导的代谢紊乱
为明确LRRC7⁺星形胶质细胞的热记忆是否直接驱动代谢紊乱,研究利用rAAV病毒特异性标记并分选LRRC7⁺星形胶质细胞,将其移植至小鼠PVN(图3A–B)。移植细胞可成功定植且无明显炎症。9周HFD喂养后,接受LRRC7⁺星形胶质细胞的小鼠体重、内脏脂肪显著升高,糖耐量与胰岛素敏感性进一步恶化(图3C–E)。在小鼠体重分化前,对两组小鼠进行为期4周的HFD喂养,结果发现,LRRC7⁺组已出现能量消耗降低、呼吸交换率升高(图3F–G);eWAT的脂肪酸氧化、脂质代谢与GPCR-cAMP通路基因显著下调,脂解关键蛋白ATGL、p-HSL及基础甘油释放均明显降低(图3H–I)。
为验证LRRC7⁺星形胶质细胞对热记忆的调控作用,研究向小鼠PVN注入抑制型化学遗传学受体病毒,并在二次热应激期间使用氯氮平-N-氧化物(CNO)特异性沉默LRRC7⁺星形胶质细胞(图3J)。钙信号记录显示,CNO可快速降低星形胶质细胞Ca²⁺活动(图3K),并几乎完全消除热记忆召回,使热记忆相关染色质可及性与特征评分显著下降(图3L–M)。功能上,抑制LRRC7⁺星形胶质细胞可显著减轻HFD诱导的肥胖、脂肪堆积与胰岛素抵抗,恢复能量消耗与脂质利用效率(图3N–R),且不影响摄食与活动。同时,脂解功能与相关蛋白表达也得到明显改善。
综上,LRRC7⁺星形胶质细胞携带的热记忆可长期调控全身代谢稳态。
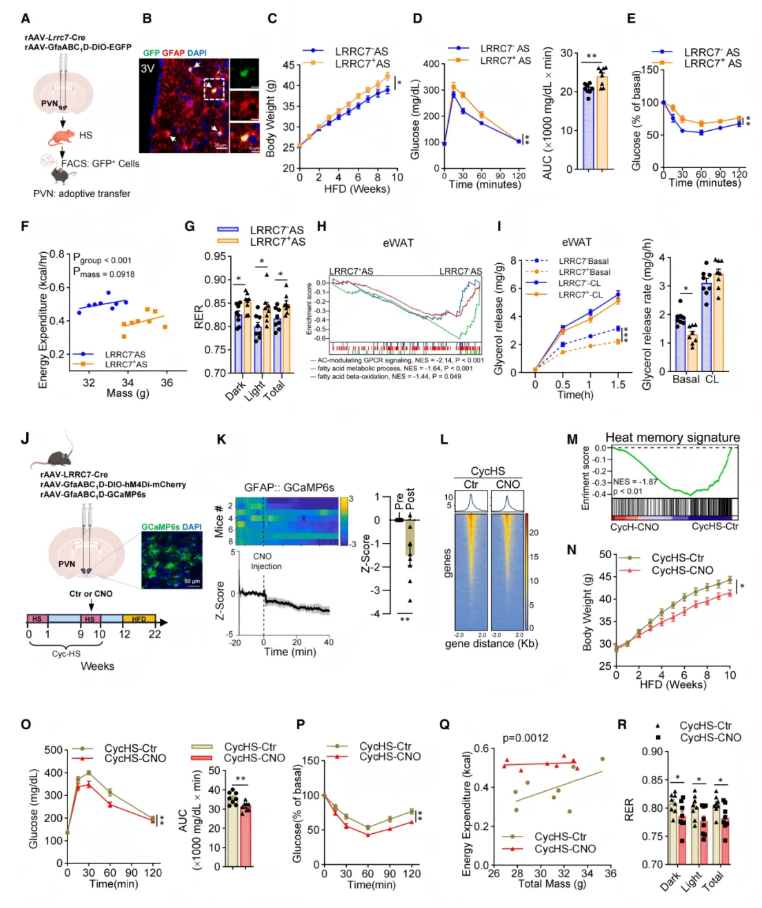
图3.LRRC7⁺星形胶质细胞的热记忆使小鼠易患饮食诱导的代谢紊乱
04.LRRC7⁺星形胶质细胞在热应激时被皮肤来源的KLK14标记
热应激可显著改变血清蛋白谱,但其诱导的循环因子是否参与LRRC7⁺星形胶质细胞的热记忆形成尚不明确。研究将HS或PF小鼠血清输入幼稚受体小鼠,发现HS血清可显著扩增LRRC7⁺星形胶质细胞,热灭活后该效应消失,提示关键刺激为热不稳定性蛋白。血清蛋白质组筛选出4种持续升高的分泌蛋白,仅KLK14可进入下丘脑,可能是介导星形胶质细胞扩增的关键因子(图4A–E)。ELISA显示,KLK14仅在37℃热应激后升高,呈温度依赖性;外卖骑手的KLK14水平也随高温暴露上升,皮肤角质形成细胞是其主要来源。
为验证KLK14的作用,研究对小鼠给予重组KLK14(rKLK14)处理,发现其可特异性扩增下丘脑第2亚群星形胶质细胞,转录谱与热应激诱导的LRRC7⁺细胞高度一致,并显著增加PVN区LRRC7⁺星形胶质细胞比例(图4F–J)。rKLK14可在体内抑制脂肪脂解,但对体外脂肪细胞无直接作用,说明其通过中枢发挥代谢效应。
进一步构建皮肤特异性KLK14敲除小鼠(Klk14K14-KO),发现皮肤敲除KLK14可完全阻断热应激诱导的循环KLK14升高、LRRC7⁺星形胶质细胞扩增及热记忆相关染色质开放,同时提高能量消耗、促进脂肪脂解相关通路与蛋白表达(图4K–T)。
通过质谱与测序筛选,研究确定细胞黏附分子CHL1是KLK14在LRRC7⁺星形胶质细胞上的功能受体。体外实验证实二者直接结合,星形胶质细胞敲低CHL1可明显缓解KLK14诱导的代谢紊乱。
以上结果表明,皮肤来源的KLK14通过作用于LRRC7⁺星形胶质细胞的CHL1受体印记热记忆,使机体更易发生代谢紊乱。
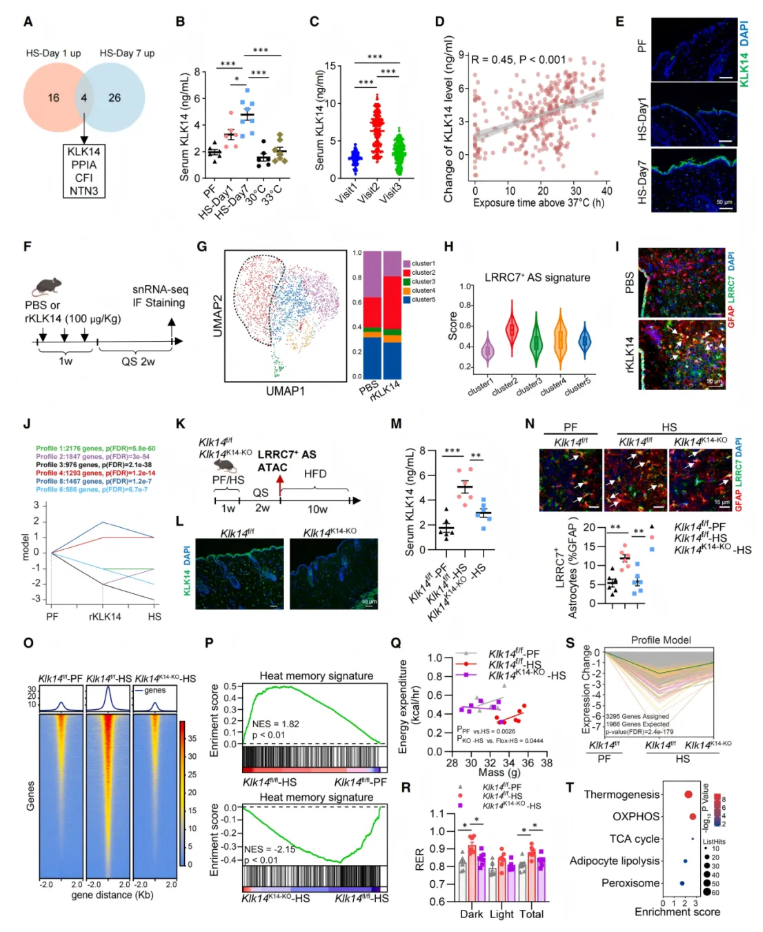
图4.LRRC7⁺星形胶质细胞在热应激时被皮肤来源的KLK14标记
05.ALKBH1控制LRRC7⁺星形胶质细胞中KLK14诱导的表观遗传记忆
KLK14可通过CHL1印记LRRC7⁺星形胶质细胞的热记忆,但其下游表观遗传机制仍不明确。对rKLK14处理的星形胶质细胞进行RNA-seq发现,表观调控因子Alkbh1可被KLK14-CHL1通路显著上调(图5A)。ALKBH1可介导DNA N6-甲基腺嘌呤(N6-mA)去甲基化;rKLK14处理后,PVN星形胶质细胞N6-mA水平明显降低(图5B)。
为验证其功能,研究构建星形胶质细胞特异性Alkbh1GFAP-KO小鼠(图5C–D)。ATAC-seq与N6-mA DIP-seq联合分析显示,敲除Alkbh1可抑制2546个rKLK14诱导的染色质开放位点,且开放区域与N6-mA峰呈负相关(图5E–F)。KEGG分析表明,相关基因富集于GABA能突触等神经元功能通路(图5G);Alkbh1缺失可显著降低LRRC7⁺星形胶质细胞的热记忆评分(图5H)。
功能表型显示,星形胶质细胞Alkbh1敲除可逆转rKLK14导致的能量消耗下降,恢复脂肪脂解能力(图5I–J),且不影响摄食与活动。HFD喂养10周后,Alkbh1^GFAP-KO小鼠的体重增加、脂肪堆积、糖耐量受损及胰岛素抵抗均显著改善(图5K–M)。
综上,ALKBH1通过N6-mA去甲基化调控KLK14诱导的LRRC7⁺星形胶质细胞表观遗传记忆。
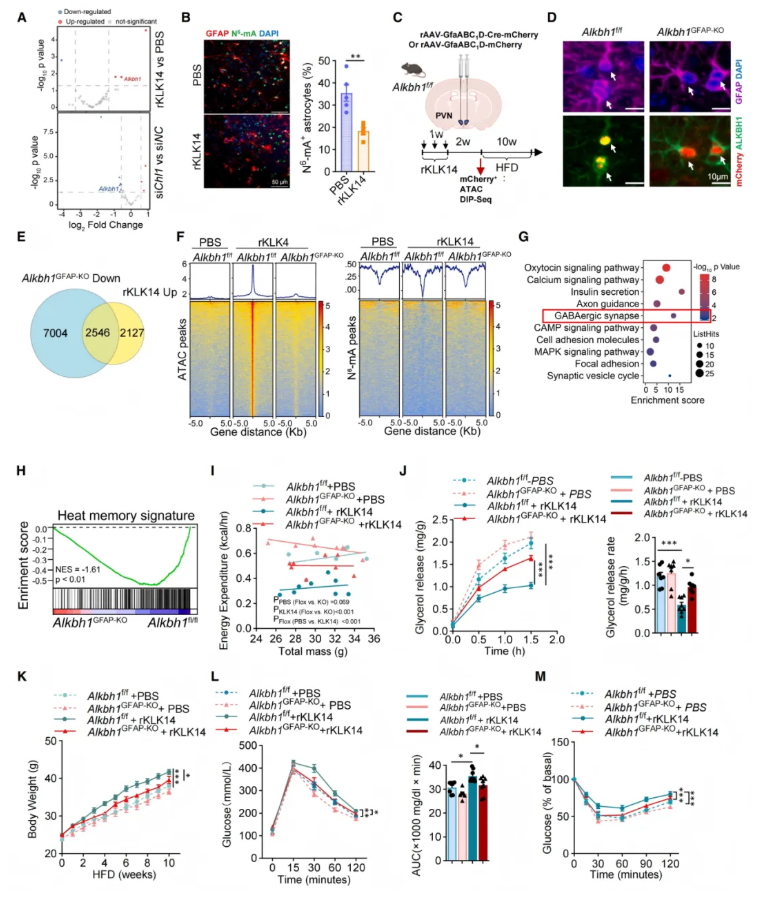
图5.ALKBH1控制LRRC7⁺星形胶质细胞中KLK14诱导的表观遗传记忆
06.LRRC7⁺星形胶质细胞抑制PVNOXT神经元-SNS回路以驱动内脏脂肪沉积
已有证据提示LRRC7⁺星形胶质细胞可能通过GABA调控神经元活性,但具体神经环路尚不明确。研究发现,rKLK14可显著上调星形胶质细胞中GABA合成关键酶Maob的表达,该作用依赖CHL1与ALKBH1介导的N6-mA修饰。
体内钙成像显示,激活LRRC7⁺星形胶质细胞可显著抑制邻近PVN神经元活性(图6A–B)。逆行示踪与免疫荧光证实,PVNOXT神经元直接支配eWAT,并与LRRC7⁺星形胶质细胞空间邻近(图6C–E)。电生理结果显示,LRRC7⁺星形胶质细胞可产生TTX(河豚毒素,阻断神经元动作电位)不敏感、GBZ(加巴嗪,GABAₐ受体拮抗剂)敏感的紧张性GABA电流,证实其通过非突触释放GABA抑制PVNOXT神经元(图6F–H)。
进一步移植实验表明,LRRC7⁺星形胶质细胞可显著增强PVNOXT神经元的紧张性GABA电流,且不依赖神经元放电(图6I–L),确认其通过GABA直接抑制OXT神经元。
功能上,LRRC7⁺星形胶质细胞可降低eWAT交感神经支配与去甲肾上腺素(NE)水平;而激活PVNOXT神经元可逆转上述效应,这一作用可被交感神经毒素6-OHDA阻断(图6M–O)。
综上,本研究揭示一条LRRC7⁺星形胶质细胞—PVNOXT神经元—交感神经的脑-脂肪环路,通过调控GABA释放控制脂肪脂解。
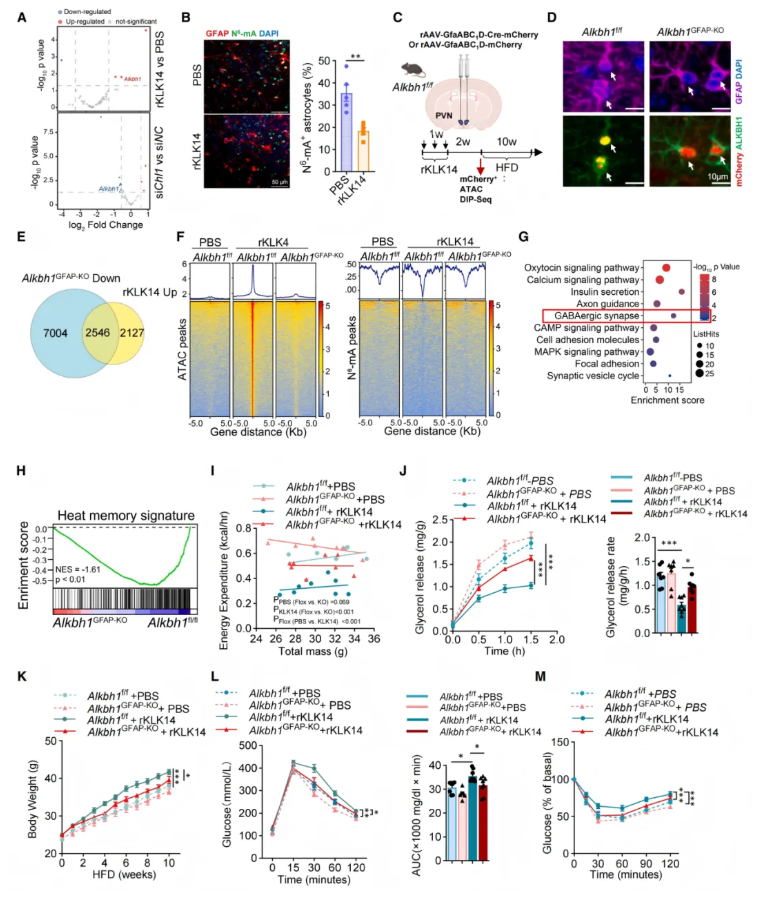
图6.LRRC7⁺星形胶质细胞抑制PVNOXT神经元-SNS回路以驱动内脏脂肪沉积
07.维生素A改善热应激暴露小鼠和人类的KLK14水平并缓解代谢紊乱
鉴于皮肤-下丘脑轴在热记忆相关代谢紊乱中的关键作用,研究探索了维生素A对皮肤稳态与代谢的影响。皮肤单细胞测序显示,热应激会下调角质形成细胞的视黄酸通路,并降低皮肤视黄醇水平(图7A–B);体外实验证实,维生素A可抑制高温诱导的KLK14表达(图7C)。
动物实验显示,热应激期间补充维生素A可降低血清KLK14水平、减少PVN区LRRC7⁺星形胶质细胞扩增,并提升能量消耗、改善脂质利用与脂肪脂解(图7D–I)。持续高脂饮食后,维生素A显著缓解热应激介导的体重增加、糖代谢异常与脂肪堆积(图7J)。
临床随机对照试验纳入59名外卖骑手,给予维生素A(5000 IU/日)或安慰剂干预。结果显示,维生素A可显著抑制热暴露引起的KLK14升高,并减少BMI、腰围、腹部内脏脂肪及胰岛素抵抗的增幅(图7K–R),且对血压无明显影响。
综上,维生素A可通过抑制KLK14生成,在小鼠和人类中缓解热应激相关代谢紊乱。
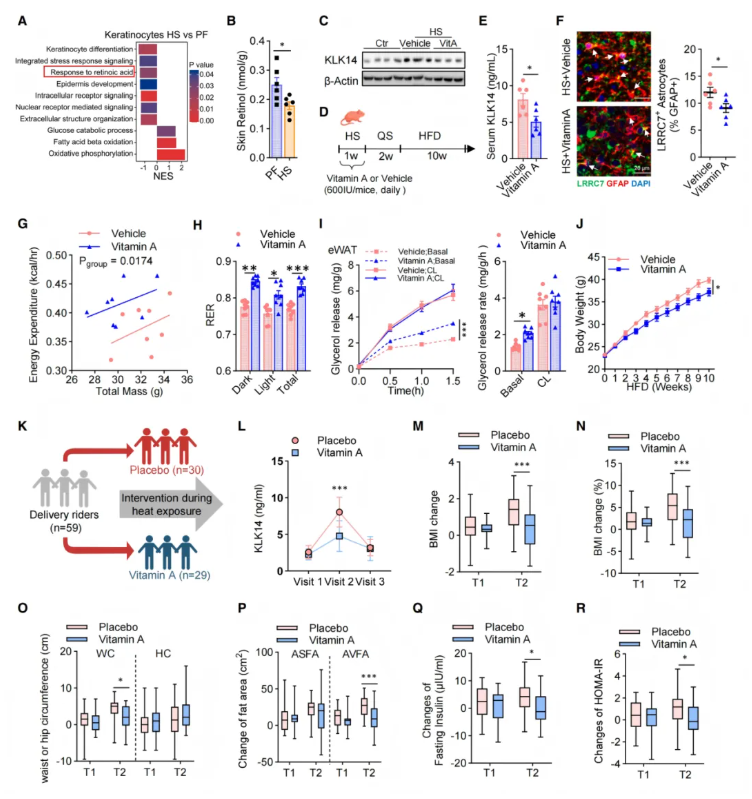
图7.维生素A改善热应激暴露小鼠和人类的KLK14水平并缓解代谢紊乱
研究总结
该研究揭示了热应激通过皮肤-下丘脑轴驱动长期代谢功能障碍的全新机制。在全球变暖背景下,热应激与慢性代谢疾病的关联机制尚不明确。本研究通过动物模型与临床队列结合发现,热应激可诱导皮肤角质形成细胞分泌KLK14,该蛋白经血液循环进入下丘脑,通过受体CHL1特异性作用PVN的LRRC7+星形胶质细胞,并经ALKBH1介导的DNA N6-mA去甲基化完成表观遗传重编程,形成稳定可召回的热记忆。携带热记忆的星形胶质细胞可抑制下游神经环路,进而加剧高脂饮食诱导的肥胖与胰岛素抵抗。此外,补充维生素A可有效缓解小鼠及人群中热应激相关的代谢紊乱,为全球变暖带来的代谢疾病防控提供了全新靶点与低成本干预策略。









