

标题:GSDME/IL-18 pyroptotic axis prevents myosteatosis by expanding tissue-resident macrophages to promote muscle regeneration
发表期刊:Journal of Clinical Investigation
影响因子:13.6
客户单位:海军军医大学
百趣提供服务:经典脂质组学
研究背景
代谢-炎症串扰调控肌肉修复过程。尽管细胞焦亡通常会加重无菌性损伤,但本研究证实,髓系细胞募集相关的GSDME依赖性细胞焦亡信号通路,却反常地促进了组织再生。机制研究表明,GSDME下游的IL-18可在TRMs中激活KLF4/JUN信号通路,从而维持其组织修复与脂质清除能力。该GSDME/IL-18-TRMs轴在衰老肌肉中功能受损,但外源性补充IL-18可逆转肌脂肪变性并加速肌肉再生。
研究表明GSDME依赖性细胞焦亡信号可作为代谢检查点,通过维持TRMs驱动的脂质稳态,进而支持肌肉组织的再生修复。
图形摘要
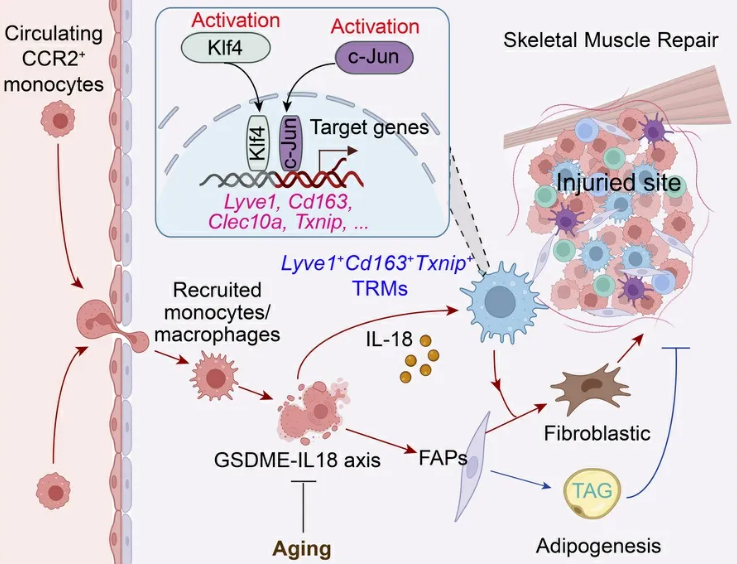
研究结果
01.GSDME参与骨骼肌损伤应答并为肌肉再生所必需
为探究Gasdermin家族蛋白在手术应激状态下骨骼肌中的潜在作用,分析了初次胆道手术后5-8天因胆汁漏而需要再次手术的患者的腹直肌样本。在所有 Gasdermin家族成员中,GSDME mRNA在骨骼肌中呈现最为显著的上调(图1A-B)。电镜观察显示,损伤肌纤维周边可见大量发生细胞膜破裂的细胞(图1C)。在Gasdermin家族中,Gsdme在损伤肌肉中上调幅度最为显著(图1D),同时伴随GSDME蛋白及其上游caspase 3发生明显剪切活化(图1E)。
随后在Gsdme全身敲除小鼠(KO)及野生型小鼠(WT)中,于损伤3个时间点(图1F)检测肌肉修复情况。至D14时,WT对照组已完全恢复,而KO小鼠仍表现出多种病理表型,包括校正体重后的腓肠肌质量下降(图1G)、损伤肌肉组织中大量脂质蓄积(图1H)以及握力显著降低(图1I)。组织学检测显示,与WT小鼠相比,GSDME KO小鼠的组织损伤更为严重(图1J左图)。CTX损伤后GSDME KO小鼠肌纤维体积显著减小(图1J右图),提示缺失GSDME会导致肌肉再生能力受损。上述结果通过荧光ATP检测得到进一步验证(图1K)。油红O与围脂滴蛋白1(perilipin 1)染色显示,KO肌肉中脂肪替代现象显著增加(图1L)。上述结果证实GSDME缺失会显著损害骨骼肌修复进程,其潜在机制可能与代谢稳态紊乱及脂质异常蓄积相关。
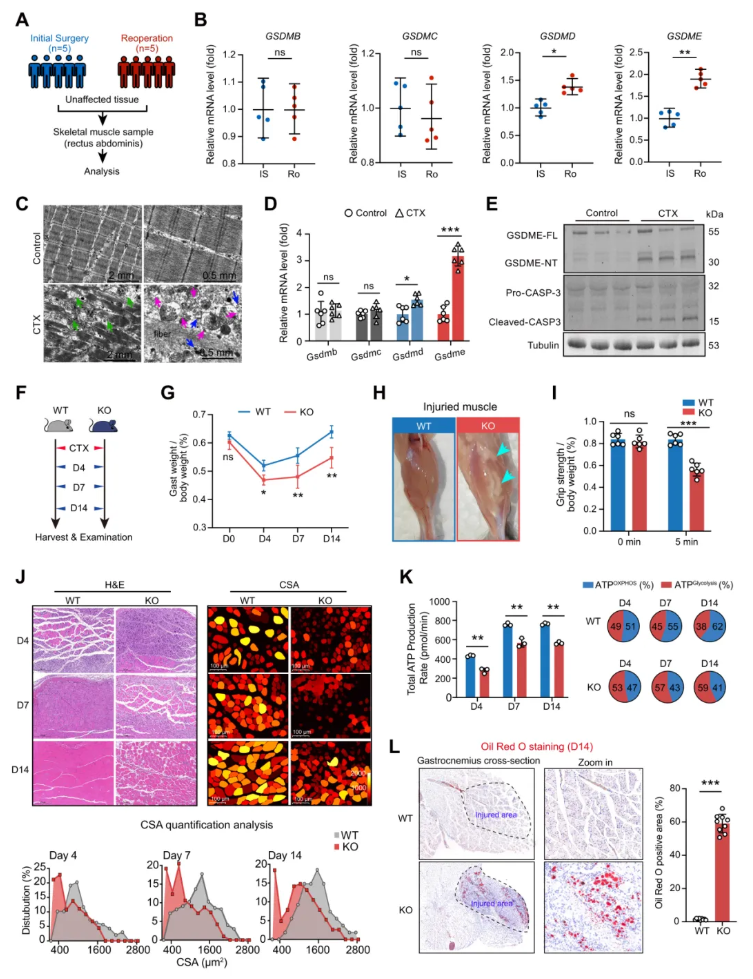
图1.GSDME在损伤骨骼肌中被激活,其敲除可通过诱发代谢紊乱与脂肪蓄积阻碍组织修复
02.批量转录组测序与脂质组学证实GSDME缺失介导肌脂肪变性
为验证骨骼肌修复受损与肌内脂质蓄积之间的关联,通过对WT和GSDME KO小鼠在CTX损伤后D4、D7、D14三个时间点的骨骼肌进行了时序批量RNA 测序分析(图2A)。主成分分析显示,不同时间点及不同基因型之间存在显著差异的转录组谱(图2B)。KO与WT肌肉间的差异表达基因,如图2C所示。利用Mfuzz算法鉴定出6个在两组中均具有相似时序表达模式的动态转录簇(簇1–5和簇7),唯有簇6呈现出独特的基因表达特征(图2D)。基因网络分析表明,在WT肌肉中,簇6主要参与肌发生、合成代谢等再生相关过程;而在KO肌肉中,该簇则与脂肪生成及脂质重塑通路相关(图2E)。
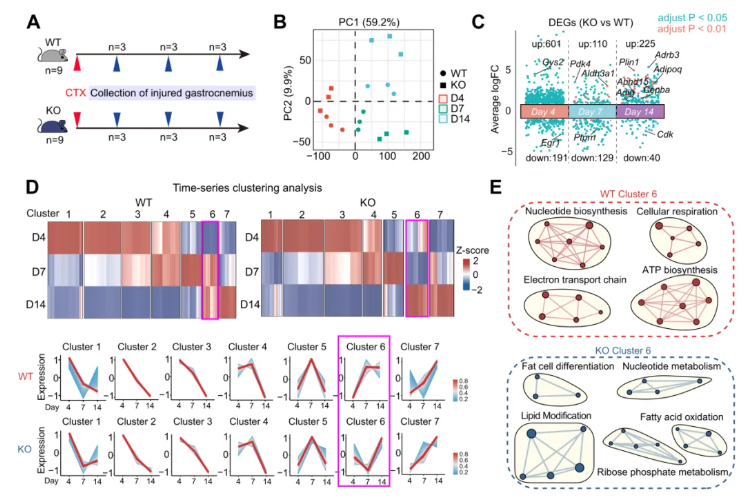
图2. 时序转录组分析揭示Gsdme缺失促进肌内成脂
为进一步明确GSDME缺失所导致的脂质蓄积谱,开展基于质谱的非靶标脂质组学分析(图3A)。脂质组学数据显示分组区分度良好,模型构建稳定可靠(图3B)。在鉴定出的脂质分子中,TAG、PC和PE含量最为丰富(图3C)。
在KO小鼠肌肉中,共有726种脂质上调、295种脂质下调(图3D)。KEGG通路分析显示,上调脂质主要富集于脂质代谢、脂肪消化与吸收通路,而下调脂质则与亚油酸、花生四烯酸代谢相关(图3E)。
值得注意的是,TAG、PC、SHexCer以及HC/NDS在KO小鼠中上调最为显著(图3F)。
WT和KO小鼠之间饱和TAG水平相似,但KO肌肉中单、双和三不饱和TAG水平显著更高(图3G)。而长链TAG在KO肌肉中显著升高(图3H)。
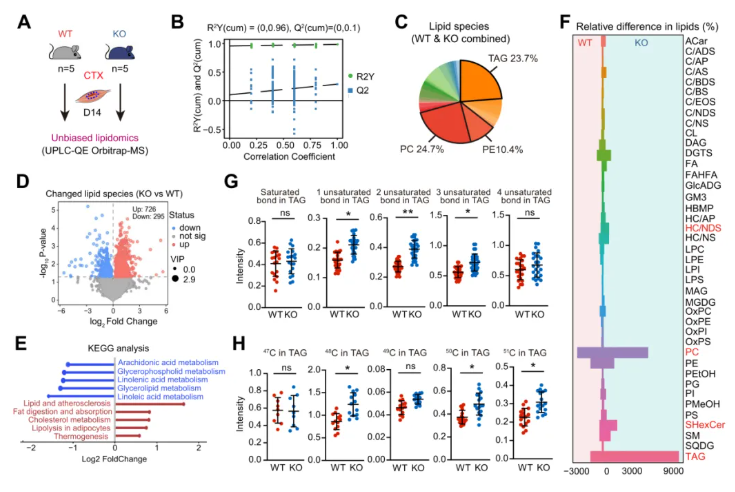
图3. 脂质组学揭示Gsdme缺失促进肌内TAG富集
03.单细胞RNA测序揭示GSDME-KO小鼠肌肉中免疫-基质细胞重编程
经质控后,对WT和KO小鼠损伤骨骼肌中的13,432个细胞进行测序分析,并将其进行聚类(图4A)。KO小鼠中FAPs和巨噬细胞比例显著升高(图4B)。进一步分析显示,KO小鼠中FAPs-巨噬细胞间相互作用显著增强(图4C-D)。配体-受体互作分析显示,KO小鼠Mif和Lgals9介导的细胞互作减弱,而趋化因子、Tgfβ及Tnf介导的信号互作显著增强(图4E)。
巨噬细胞对FAPs清除的调控是肌肉正常修复的关键环节,因此进一步对FAPs和巨噬细胞进行亚群分群,以探究其转录水平变化。共鉴定出7个FAPs亚群(图4F)根据标志基因判断,FAPs-0具有显著的成脂分化倾向,而FAPs-2为成纤维细胞样亚群。KO小鼠中成脂性FAPs-0比例升高,成纤维样FAPs-2比例降低(图4G)。拟时序分析提示,Pi16⁺Dpp4⁺FAPs-4可能为初始状态FAPs,而FAPs-2处于终末分化状态(图4H)。GO富集分析进一步证实,FAPs-0主要参与脂肪分化过程,而FAPs-2主要参与创面修复(图4I)。
巨噬细胞被聚为4个亚群(图4J)。与WT小鼠相比,KO小鼠Mφ-0比例升高、Mφ-1比例降低(图4K)。而以Ccr2高表达为标志的Mφ-3,大概率是由招募的单核细胞分化而来的巨噬细胞亚群(图4L)。GO富集分析显示,Mφ-1显著富集于组织修复与骨骼肌发育相关通路;而Mφ-0、Mφ-2、Mφ-3则主要与炎症反应和白细胞迁移相关(图4M)。此外,Mφ-3还与细胞死亡调控相关(图4M)。多重免疫组化染色显示,损伤组织内存在大量LYVE1⁺CD11b⁺组织驻留巨噬细胞,而在KO小鼠中该类细胞数量显著减少(图4N)。
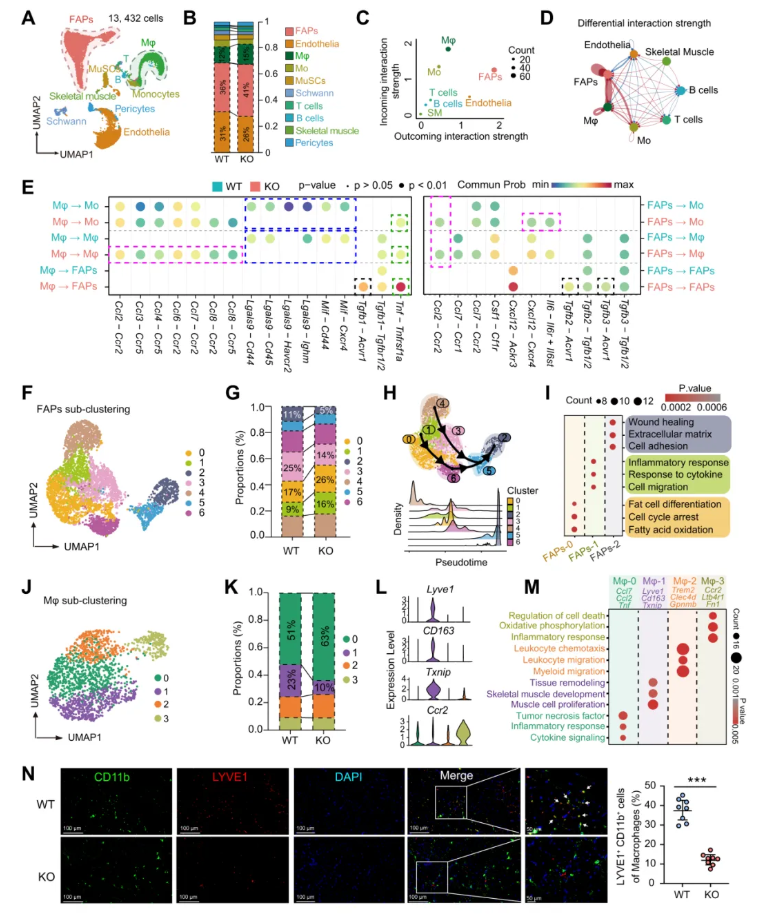
图4. 单细胞测序揭示GSDME协同调控TRMs与FAPs
04.巨噬细胞中的GSDME而非FAPs对骨骼肌再生至关重要
对野生型(WT, GsdmeWT/WT)、GsdmeS/S、GsdmeS/S FR及GsdmeS/S MR小鼠进行CTX诱导的骨骼肌损伤造模。与GSDME KO小鼠相似,GsdmeS/S与GsdmeS/S FR小鼠腓肠肌重量显著降低,而GsdmeS/S MR小鼠肌肉重量与WT小鼠无显著差异(图5A)。
GsdmeS/S与GsdmeS/S FR小鼠损伤肌肉出现明显脂肪替代,运动能力下降;而GsdmeS/S MR小鼠未出现上述表型(图5B-C)。H&E染色/肌纤维横截面积分析(图5D)、SDH染色(图5E)及IIa/IIb型肌纤维比例(图5F)均得到一致结果。GsdmeS/S与GsdmeS/S FR小鼠CD45⁺白细胞数量显著升高,而GsdmeS/S MR小鼠升高幅度明显降低(图5G)。
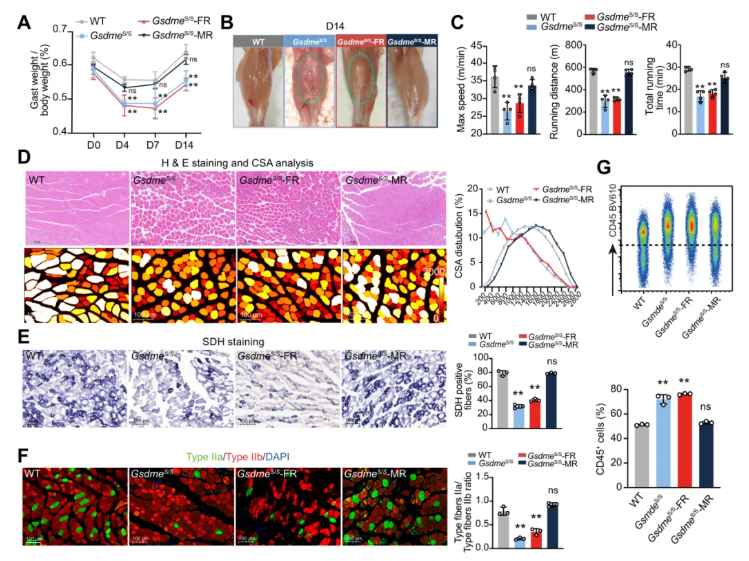
图5. 招募巨噬细胞而非FAPs的GSDME介导骨骼肌修复
接下来探究上述修复缺陷是否与细胞代谢改变及髓系细胞动力学异常相关。Seahorse代谢分析显示,与WT小鼠相比,GsdmeS/S和GsdmeS/S-FR小鼠肌肉的氧耗速率曲线显著降低,而GsdmeS/S-MR小鼠则无此变化(图6A)。对损伤肌肉中Ly6C⁺单核细胞与LYVE1⁺巨噬细胞的时序变化分析显示:WT小鼠中浸润的Ly6C⁺单核细胞快速达峰、LYVE1⁺巨噬细胞持续存在,而这一特征在GsdmeS/S和GsdmeS/S-FR小鼠中消失,但在GsdmeS/S-MR小鼠中得以恢复(图6B)。总ATP含量以及氧化磷酸化和糖酵解来源ATP的比例也呈现相似变化趋势(图6C-D)。
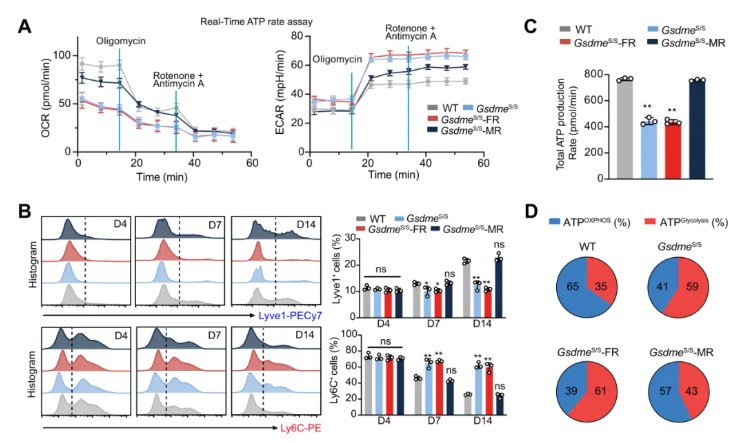
图6. Gsdme调控肌肉修复过程中的代谢重塑与巨噬细胞极化
05.GSDME缺失损害组织驻留巨噬细胞的扩增动力学
为在蛋白水平详细解析损伤肌肉中免疫细胞的特征,于损伤后三个时间点从WT和KO小鼠损伤骨骼肌中共收集1,481,156个CD45⁺白细胞,进行多重流式细胞术分析,同时结合非线性降维算法进行数据处理(图7A)。通过UMAP指导的无偏设门,将免疫细胞聚为6个亚群(图7B)多时间点分析清晰展示了损伤后免疫微环境的动态演变及GSDME缺失带来的影响(图7C)。
WT小鼠中CD45⁺白细胞浸润在D4达到峰值,至D14基本消退;而KO小鼠炎症无法正常消退,D14时仍表现为持续性白细胞浸润(图7D)。在损伤后三个时间点,GSDME KO小鼠的CD64⁺F4/80⁺巨噬细胞数量均显著高于WT小鼠(图7E)。对单核细胞Ly6C表达及巨噬细胞LYVE1染色的分析显示:KO小鼠中CCR2⁺Ly6C⁺单核细胞的下降过程(图7F)与CCR2⁻LYVE1⁺巨噬细胞的上升过程(图7G)均被显著抑制。GSDME KO小鼠巨噬细胞向促炎表型偏移:D4至D14期间持续高表达CD86、低表达CD163(图7H)。同时,cDC2数量在各基因型间无差异(图7I),提示再生受损并非由树突状细胞介导的抗原呈递异常所致。
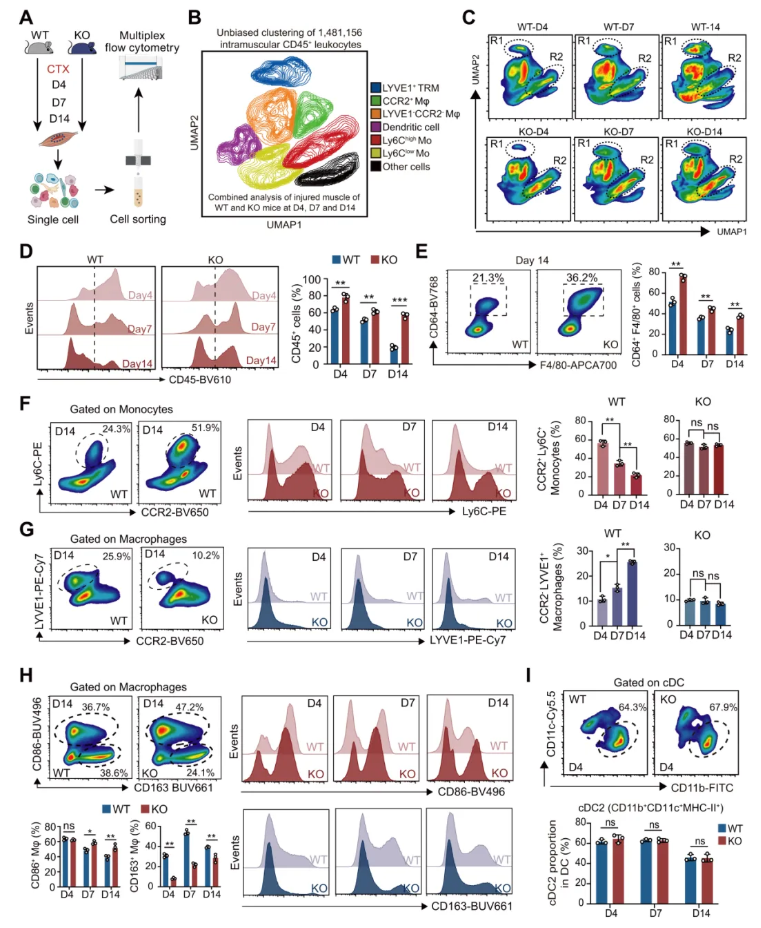
图7. GSDME调控肌内免疫细胞募集与TRMs扩增
06.GSDME缺失损害组织驻留巨噬细胞的扩增动力学
已有研究证实,GSDME介导的细胞焦亡可促进IL 1β和IL 18的释放(图8A)。中和IL 18可导致损伤肌肉出现明显脂肪替代,而中和IL 1β则无此效应(图8B);运动能力检测(图8C)也验证了这一结果。同时,阻断IL 18可显著抑制损伤后TRMs的扩增(图8D)。
为鉴定维持TRMs的关键转录因子,采用单细胞调控网络推断与聚类分析,发现KLF4和JUN是Lyve1⁺Cd163⁺Txnip⁺巨噬细胞亚群(Mφ 1)中的两个核心转录因子(图8E)。单细胞水平调控子活性分析显示,约17%巨噬细胞的KLF4和23%的JUN处于激活状态(图8F)。机制上:IL 18处理可显著升高分选巨噬细胞中KLF4和JUN的核蛋白水平(图8G);免疫荧光同样证实,中和IL 18可抑制损伤肌肉中KLF4和JUN的核定位(图8H)。染色质免疫共沉淀定量PCR证实,KLF4和JUN可直接结合于Lyve1与Cd163启动子区域,而该结合能力在GSDME KO小鼠中显著减弱(图8I-J)。使用KLF4抑制剂kenpaullone和JUN抑制剂T5224处理,均能明显减少损伤肌肉中LYVE1⁺细胞数量(图8K)。
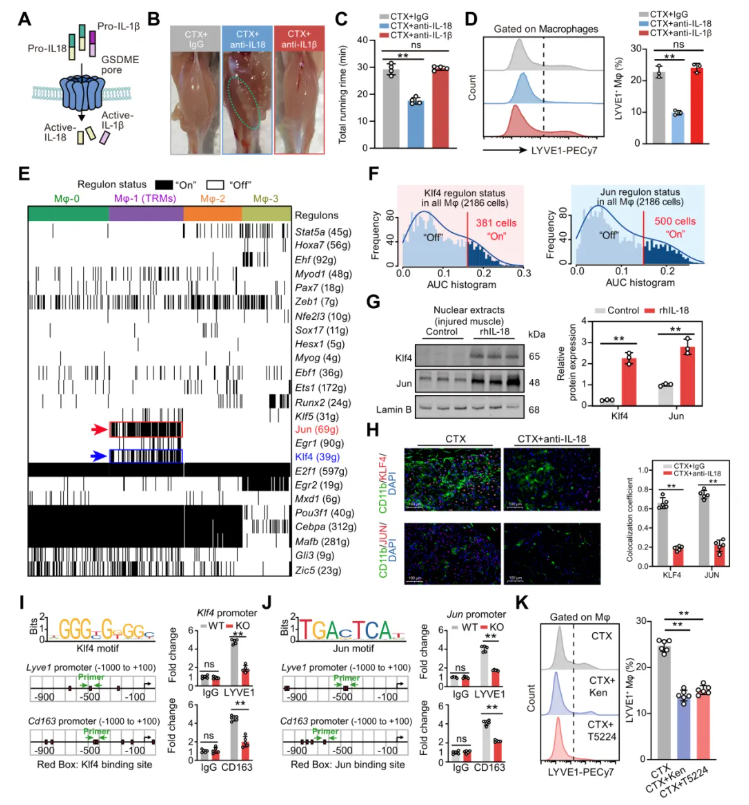
图8. GSDME通过IL-18-KLF4/JUN轴调控TRMs
07.IL-18处理可恢复GSDME信号受损的老年肌肉再生能力
衰老常伴随骨骼肌再生能力下降。为验证其功能意义,通过对年轻和老年小鼠进行CTX肌肉损伤造模,并对老年小鼠给予重组IL 18处理(图9A)。与年轻小鼠相比,老年小鼠在损伤后14天表现出明显的再生障碍,而IL 18处理可部分挽救这一缺陷(图9B-C)。同时,IL 18可恢复LYVE1⁺TRMs比例(图9D)并改善运动能力(图9E)。
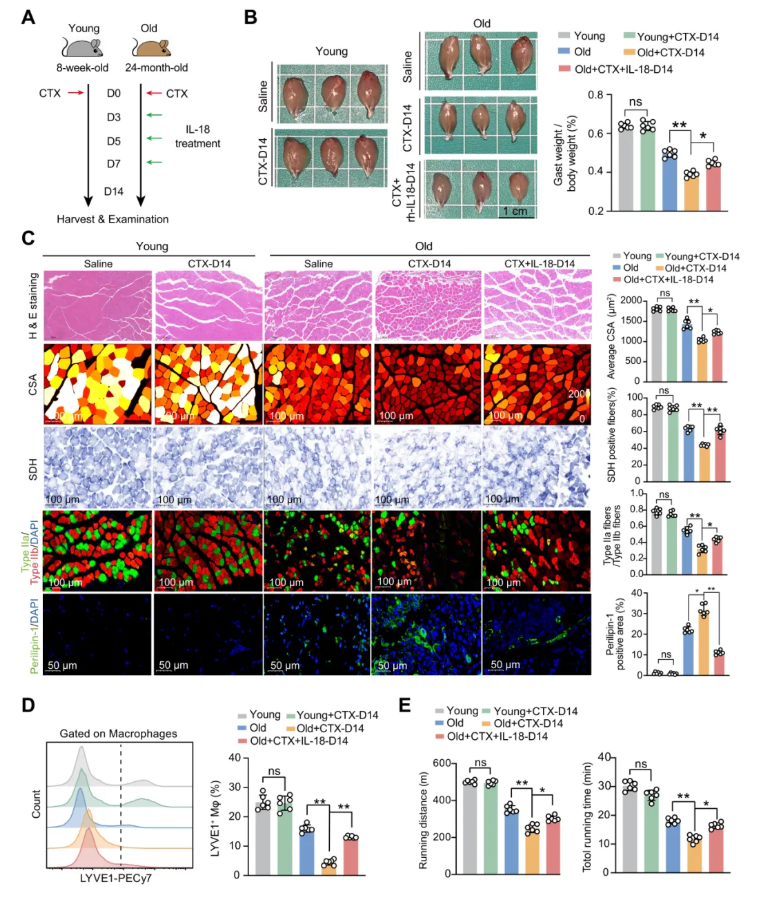
图9. IL-18挽救衰老肌肉的再生缺陷
研究总结
本研究揭示:GSDME/IL-18信号轴通过调控招募型CCR2⁺单核来源巨噬细胞中GSDME依赖性焦亡信号,构建促再生免疫微环境,进而维持TRMs扩增、抑制FAP成脂分化,并最终促进肌肉再生。该信号轴可为今后针对肌肉脂肪化、肌萎缩及衰老相关性少肌症的治疗策略提供理论基础。









