

文章标题:Taurine can restrict MtdsRNA mediated pyroptosis by enhancing mitophagy in nucleus pulposus cells
发表期刊:Cell Communication and Signaling
影响因子:8.9
客户单位:华中科技大学同济医学院附属协和医院
百趣提供服务:新一代代谢组学NGM 2 Pro、转录组测序
研究背景
腰痛主要由椎间盘退变(IVDD)引起,其与线粒体功能障碍密切相关。线粒体双链RNA(mtdsRNA)在线粒体受损时会释放至细胞质,激活RLR MAVS NLRP3通路,引发细胞焦亡及炎症。本研究发现,退变髓核组织中mtdsRNA水平升高,而细胞代谢物牛磺酸可抑制其释放。牛磺酸通过增强线粒体自噬维持线粒体稳态,从而阻断mtdsRNA介导的焦亡途径,提示mtdsRNA是治疗IVDD的潜在靶点,而牛磺酸可为IVDD的治疗提供潜在的干预策略。
研究概况
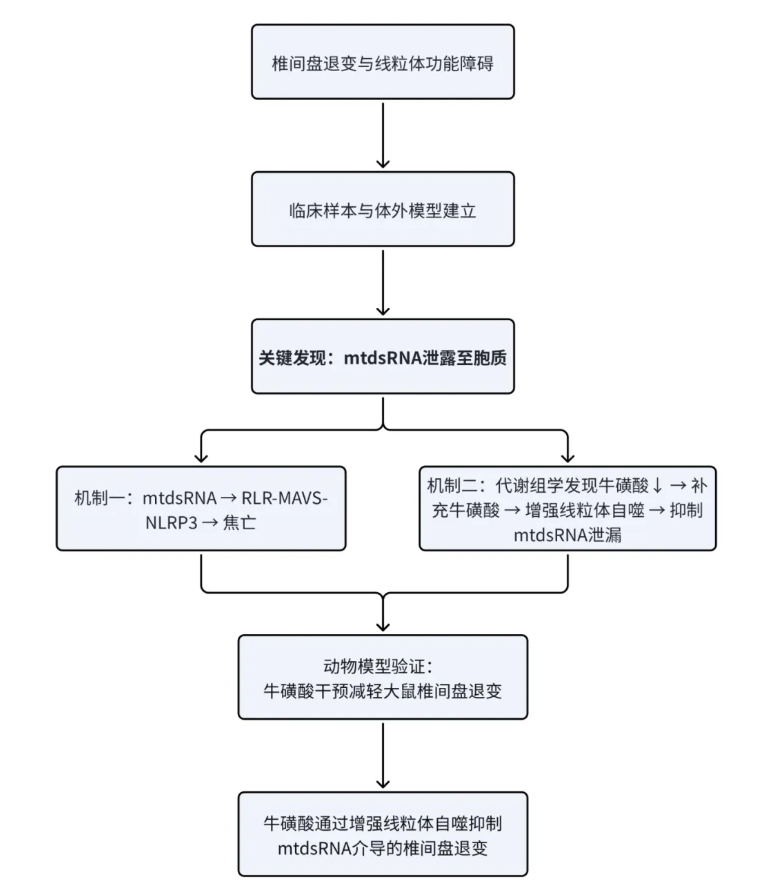
技术路线
研究结果
01.mtdsRNA在退变髓核组织中升高
为了研究mtdsRNA是否在临床退变样本中异常升高,首先对GSE245147测序数据进行了生物信息学分析。结果显示,退变髓核(NP)组织中差异表达基因包含dsRNA相关基因(如IFIT5、MX1、RIG-I、MDA5)显著上调,且Ⅰ型干扰素通路及RLR通路富集(图1a-b)。临床样本(按Pfirrmann分级)分析进一步证实,退变NP组织含水量下降、结构紊乱,同时mtdsRNA水平升高,其中ND5-L、ND6-L的升高尤为显著(图1c-e)。蛋白检测显示退变组织中PNPT1下调,RIG-I、MDA5、NLRP3表达上升,MAVS寡聚化增强,提示RLR-MAVS通路激活(图1f-g)。免疫荧光及免疫组化结果支持dsRNA与RLR蛋白共定位增加,且PNPT1下调与NLRP3升高相关(图1h-k)。综上,退变NP组织中mtdsRNA积累通过激活RLR信号通路,进而驱动炎症反应。
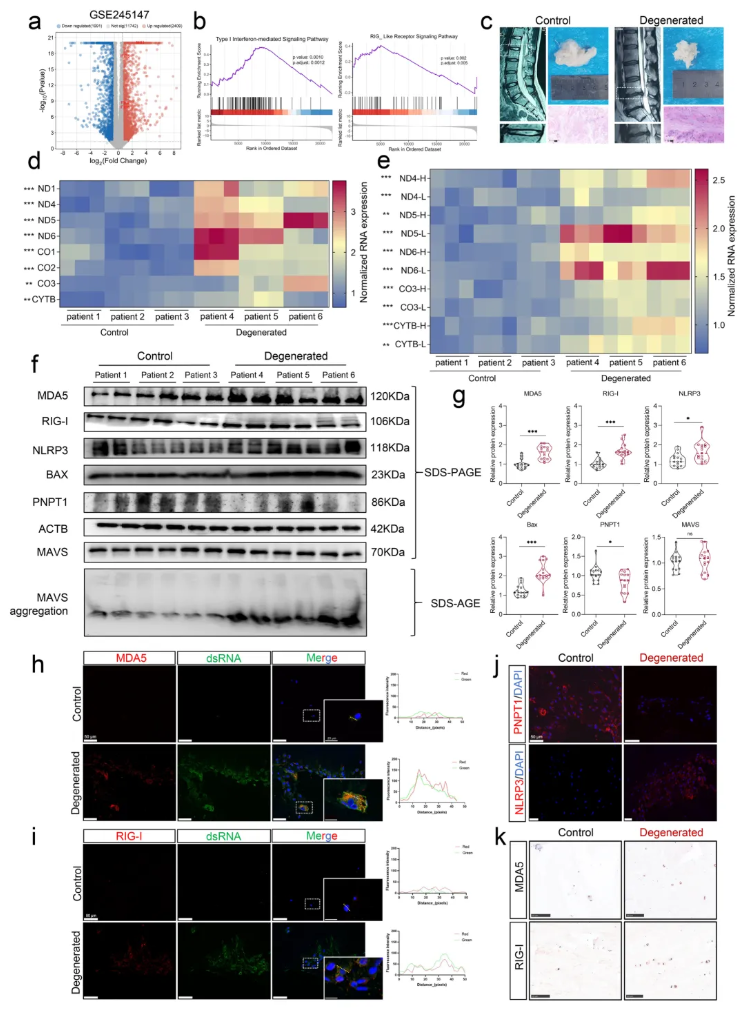
图1. mtdsRNA在退变髓核(NP)组织中表达升高
02.氧化应激促进mtdsRNA的渗漏
由于氧化应激可诱导mtdsRNA胞质逃逸,故在后续实验中使用脂多糖(LPS)刺激细胞,发现其可抑制髓核细胞(NPCs)增殖(图2a-b),破坏线粒体膜电位、增加细胞内ROS积累(图2c-f),并降低ATP水平(图2g),提示线粒体功能受损。同时,LPS下调PNPT1、上调BAX表达(图2h-l),导致mtdsRNA向胞质逃逸增加。通过qRT-PCR、链特异性PCR及RNA荧光原位杂交(FISH)证实,氧化应激下胞质mtdsRNA(特别是ND4-H/L)含量升高,且线粒体与dsRNA共定位增强(图2m-p)。结果表明,氧化应激通过损伤线粒体功能,促使mtdsRNA在胞质异常积累。
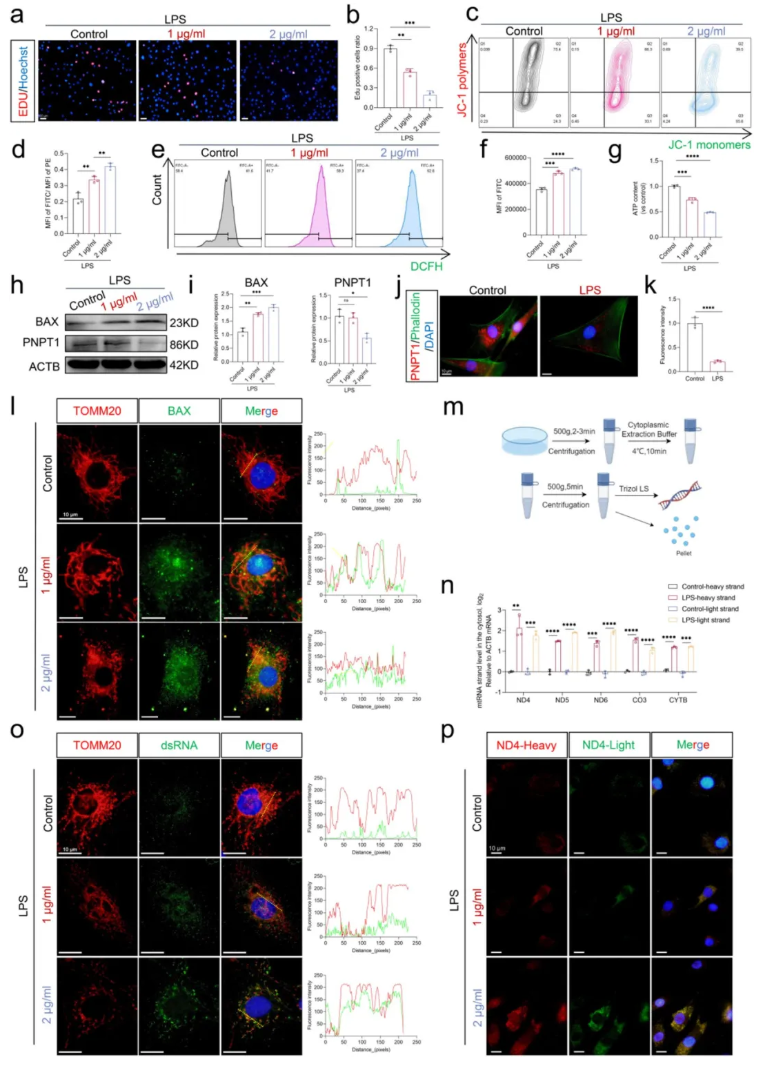
图2. 氧化应激促进mtdsRNA的渗漏
03.mtdsRNA触发RLR-MAVS-NLRP3轴并促进NPCs的焦亡
LPS诱导氧化应激激活RLR-MAVS通路并促进NPCs焦亡。为了探讨mtdsRNA与焦亡之间的关系,研究初步测定了焦亡指标。如图3a-f所示,LPS刺激可诱导NPCs发生焦亡,表现为NLRP3表达上调、CASP-1活性升高、GSDMD剪切活化、IL-1β释放增加及细胞器肿胀。同时,LPS上调RIG-I和MDA5表达,促进MAVS寡聚化,并增强RLR与MAVS的共定位(图3g-h)。RIP实验证实RIG-I和MDA5可直接结合mtdsRNA,免疫荧光实验进一步证实dsRNA与RIG-I、MDA5的共定位均增强。此外,LPS增强MAVS与NLRP3的相互作用及共定位(图3m-n)。敲低RIG-I、MDA5或MAVS均能减轻焦亡,其中MAVS敲低效果最显著,提示其在该通路中的核心作用(图3p-t)。综上,LPS刺激下mtdsRNA释放通过激活RLR-MAVS通路,进而促进NLRP3介导的焦亡。
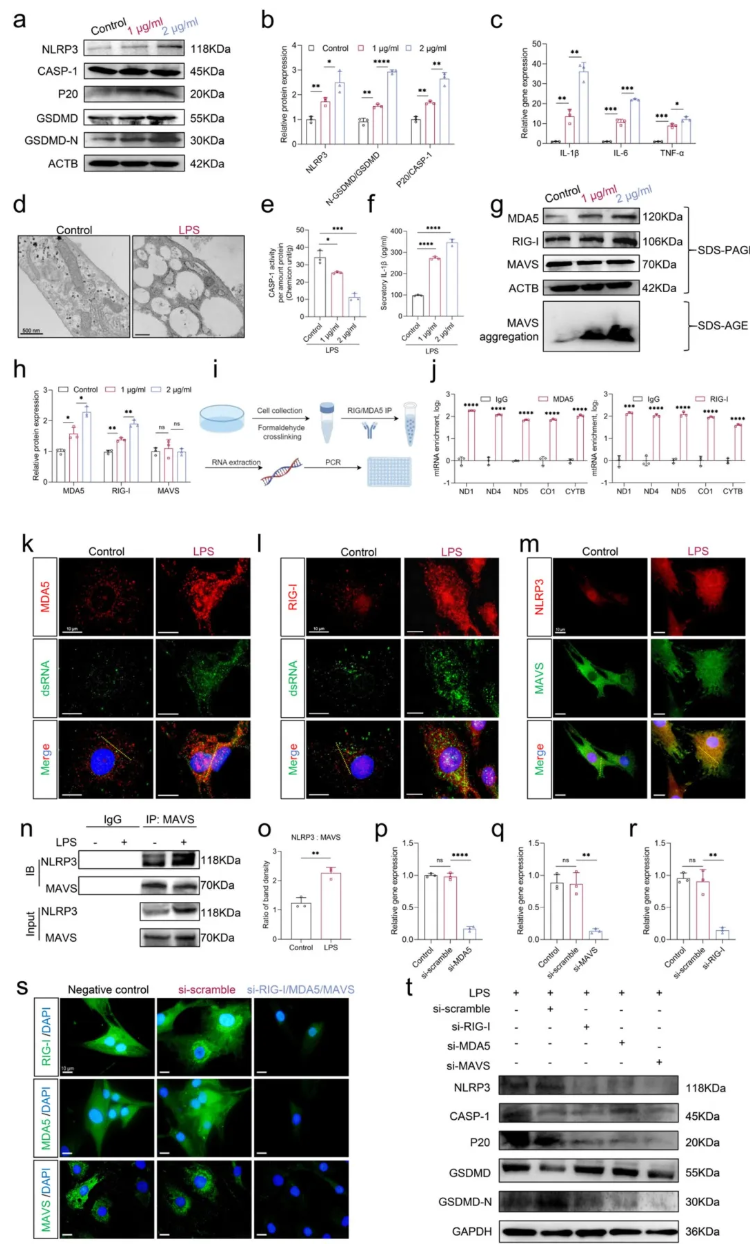
图3. mtdsRNA触发RLR-MAVS-NLRP3轴并促进NPCs的焦亡
04.抑制mtdsRNA的渗漏可以减轻NPCs的焦亡
为了探索mtdsRNA与焦亡之间的关系,随后通过PNPT1的过表达、BAX的敲低和IMT1的利用来研究焦亡的程度。图4所示,通过过表达PNPT1、敲低BAX或使用IMT1抑制mtdsRNA生成,可有效缓解LPS诱导的线粒体功能障碍,降低胞质mtdsRNA水平,进而抑制RLR-MAVS-NLRP3通路激活。这些干预措施减弱了MAVS与NLRP3的相互作用,降低CASP-1活性和IL-1β释放,从而缓解NPCs焦亡。结果表明,抑制mtdsRNA渗漏可通过阻断RLR-MAVS-NLRP3轴减轻炎症性焦亡。
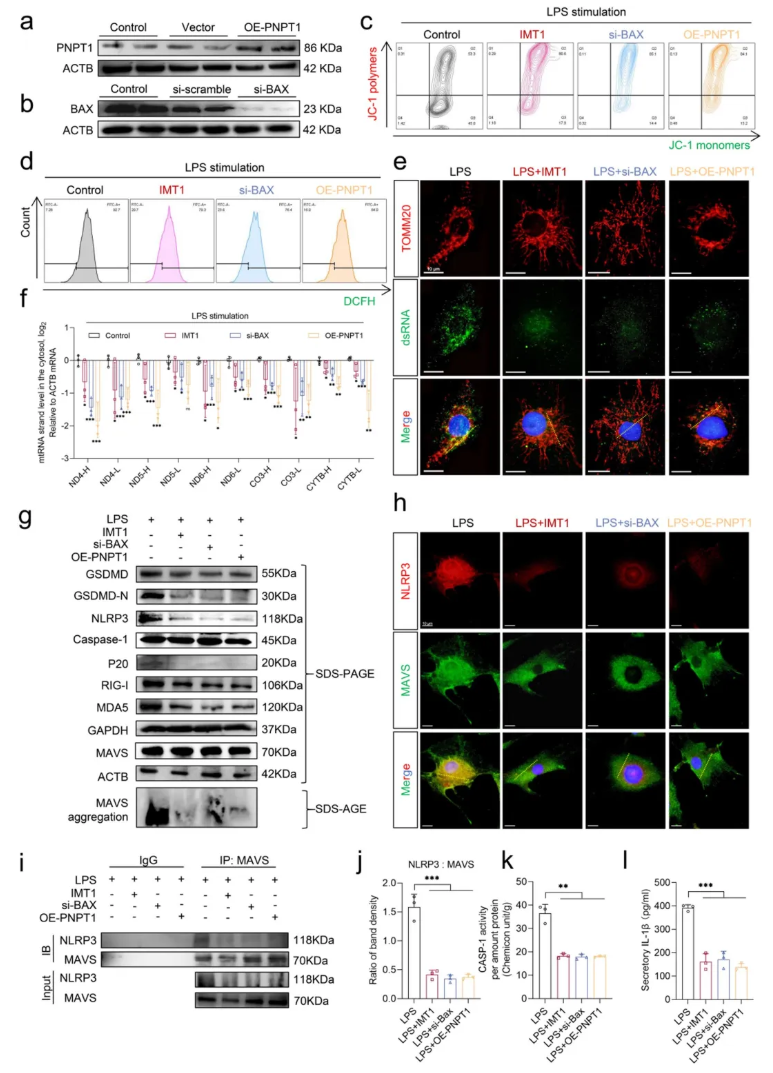
图4. 抑制mtdsRNA的渗漏可以减轻NPCs的焦亡
05.牛磺酸对于维持NPCs的线粒体功能至关重要
为了进一步了解mtdsRNA的上游调控机制,研究者采用非靶标代谢组学分析来研究代谢产物在LPS刺激下的变化。结果显示,LPS刺激导致NPCs代谢谱改变,其中牛磺酸代谢通路受影响显著(图5a-c)。LPS下调牛磺酸及其转运蛋白SLC6A6的表达,临床退变样本也证实牛磺酸含量降低且SLC6A6减少(图5d-g)。敲低SLC6A6可降低细胞内牛磺酸水平,诱导ROS积累、PNPT1下调及mtdsRNA释放,进而上调RLR表达并激活RLR-MAVS-NLRP3轴。相反,补充牛磺酸能恢复细胞内牛磺酸水平,减轻氧化应激,改善线粒体功能,抑制RLR-MAVS-NLRP3通路激活,并缓解细胞焦亡(图5h-p)。结果表明,牛磺酸缺乏通过促进mtdsRNA渗漏加剧炎症性损伤,而补充牛磺酸具有保护作用。
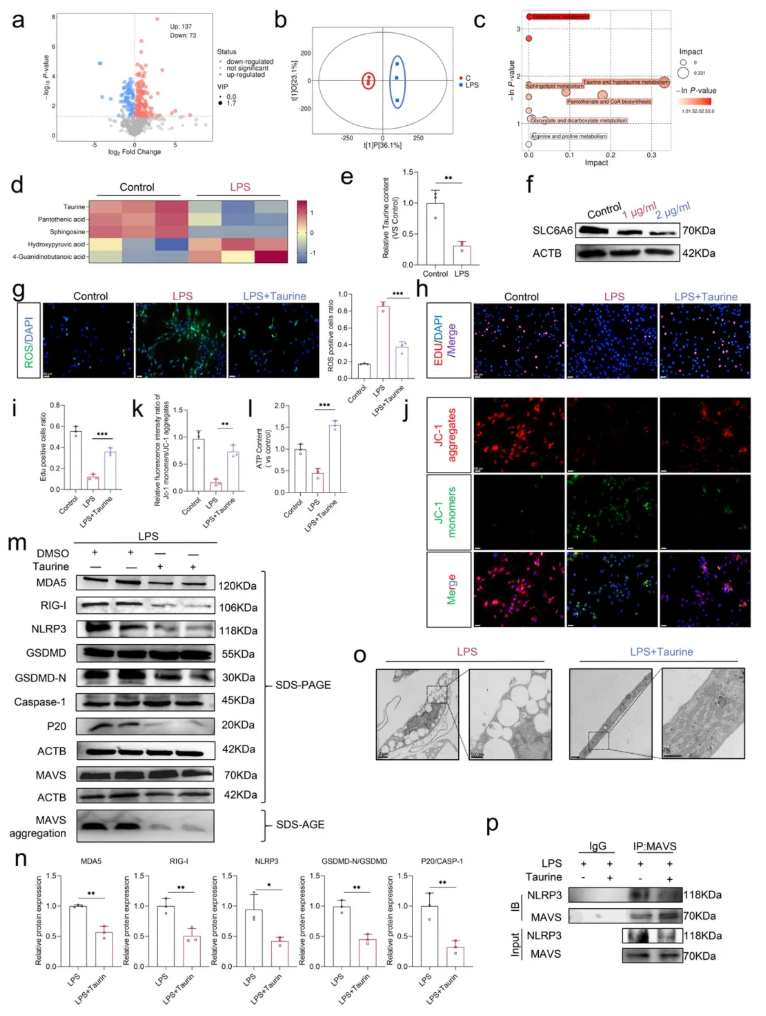
图5. 牛磺酸对于维持NPCs的线粒体功能至关重要
06.牛磺酸可以抑制mtdsRNA的渗漏
为了进一步探索mtdsRNA在牛磺酸保护作用中的重要性,在细胞被刺激前使用IMT1对其进行处理。研究发现,牛磺酸能恢复细胞活力(图6a),但该保护作用在使用IMT1抑制mtdsRNA后显著减弱。牛磺酸处理降低了胞内mtdsRNA水平,同时上调PNPT1、下调BAX表达,减少BAX与线粒体共定位(图6b-e)。图6f-k所示,即使在外源性poly(I:C)诱导mtdsRNA增加的情况下,牛磺酸仍能抑制其胞内积累,并缓解poly(I:C)介导的细胞内牛磺酸下调。RNA测序分析显示(图6i-m),牛磺酸可下调干扰素刺激基因、炎症及氧化应激相关基因的表达,同时上调ROS解毒及线粒体自噬相关基因。GSEA进一步证实牛磺酸抑制Ⅰ型干扰素通路及炎症反应,并增强抗氧化能力。综上,牛磺酸通过调节PNPT1/BAX平衡、抑制mtdsRNA释放,并激活保护性自噬通路,从而减轻氧化应激与炎症损伤。
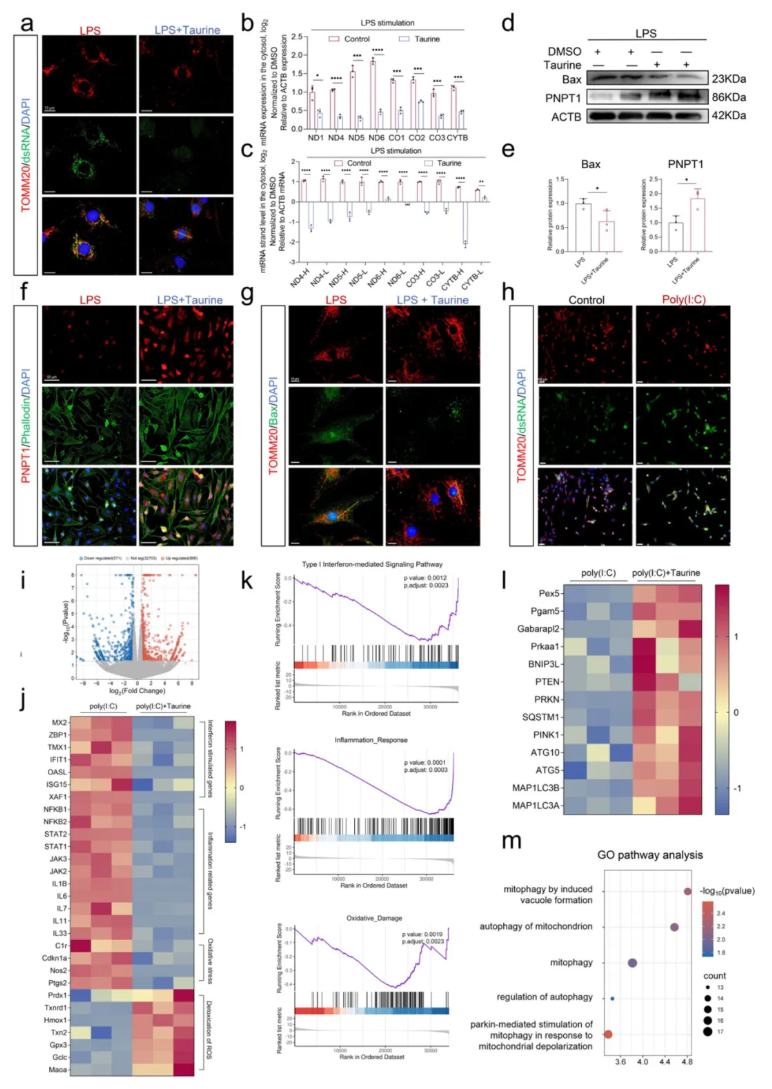
图6. 牛磺酸可以抑制mtdsRNA的泄漏
07.牛磺酸可以通过增强线粒体自噬来抑制mtdsRNA-MAVS-NLRP3轴
为探究牛磺酸调控线粒体自噬的机制,研究使用自噬抑制剂3-MA进一步观察牛磺酸对线粒体自噬的影响。如图7a-d所示,3-MA可增加ROS、降低线粒体膜电位,逆转牛磺酸的保护作用。通过mRFP-GFP-LC3腺病毒示踪及WB检测发现,牛磺酸促进自噬体形成与成熟,并激活PINK1-Parkin通路,而3-MA抑制该过程。免疫荧光进一步证实牛磺酸增强PINK1与Parkin共定位,促进受损线粒体清除。此外,抑制线粒体自噬(3-MA处理)可逆转牛磺酸对PNPT1/BAX表达及线粒体稳态的调节作用,进而导致胞质mtdsRNA积累。对RLR-MAVS-NLRP3通路的分析表明,牛磺酸通过增强线粒体自噬抑制该轴激活,而3-MA则抵消此效应(图7e-k)。综上,牛磺酸通过激活PINK1-Parkin介导的线粒体自噬,清除受损线粒体、减少mtdsRNA泄漏,进而抑制RLR-MAVS-NLRP3炎症通路。
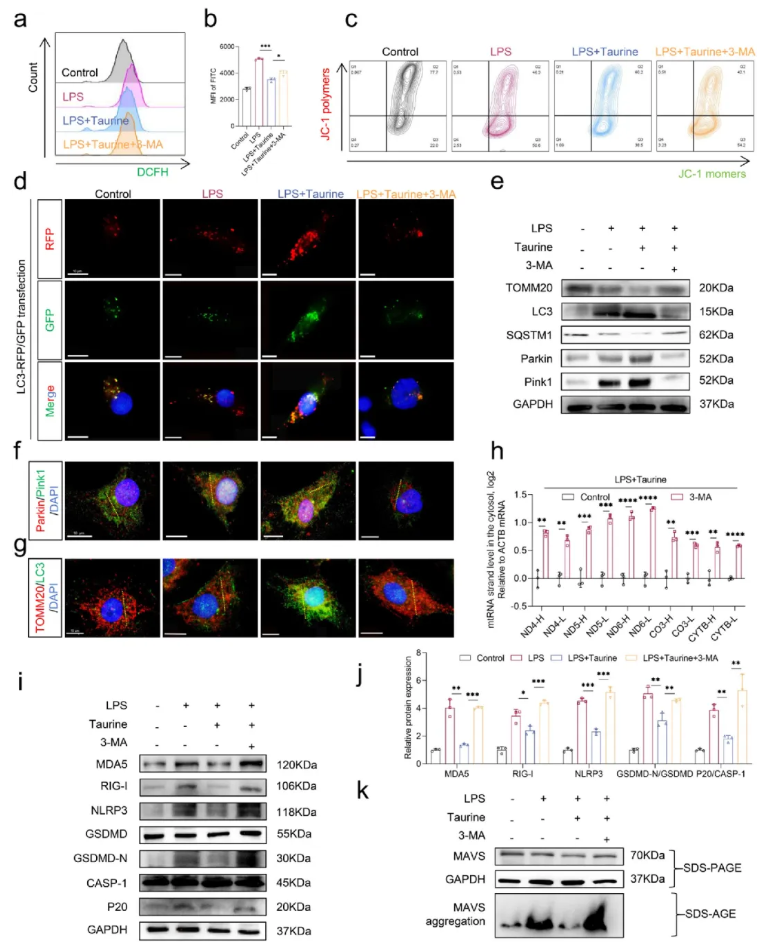
图7. 牛磺酸可以通过增强线粒体自噬来抑制mtdsRNA-MAVS-NLRP3轴
08.牛磺酸可通过抑制mtdsRNA-MAVS-NLRP3来缓解IVDD
为了建立LPS诱导的IVDD模型,向大鼠Co8/9椎间盘注射LPS,治疗组同时加入牛磺酸。一月后观察发现,牛磺酸可部分恢复LPS导致的椎间盘高度降低及MRI T2信号减弱,改善组织学结构,减少纤维化、维持髓核-纤维环边界及纤维环层状结构,改善髓核细胞聚集现象(图8a-d)。免疫组化及免疫荧光结果显示,LPS降低PNPT1、升高BAX及NLRP3表达,并增强RLR与dsRNA共定位;而牛磺酸能逆转这些变化,恢复PNPT1表达,降低BAX、NLRP3及dsRNA水平,抑制炎症通路激活(图8e-h)。综上,牛磺酸在大鼠IVDD模型中具有保护作用,能减轻椎间盘退变及炎症损伤。
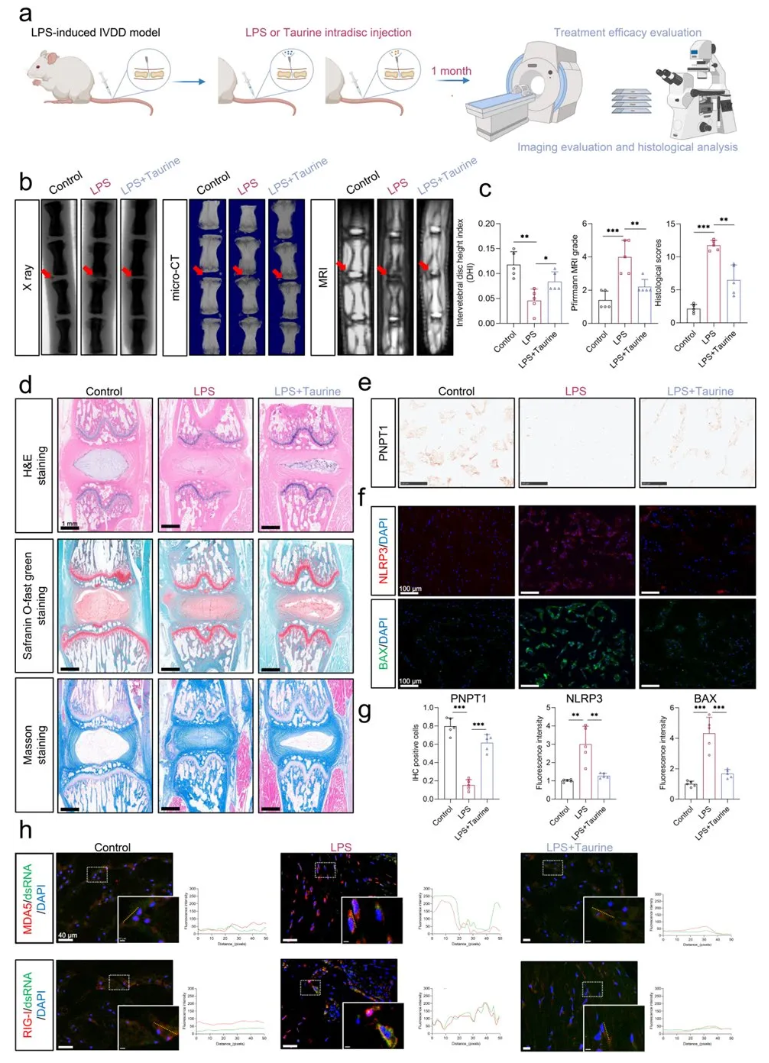
图8. 牛磺酸可通过抑制大鼠mtdsRNA-MAVS-NLRP3来缓解IVDD
研究总结
本研究揭示了mtdsRNA在IVDD中的致病机制及牛磺酸的调控作用。研究发现,退变NPCs中线粒体功能障碍导致mtdsRNA异常释放至胞质,激活RIG-I/MDA5受体并诱导MAVS寡聚化,进而招募NLRP3炎性小体,触发焦亡,进而引发炎症反应。代谢组学分析显示退变NPCs存在牛磺酸缺乏,其通过促进线粒体功能障碍加剧mtdsRNA积累。补充牛磺酸可增强线粒体自噬,抑制mtdsRNA释放,从而减轻NLRP3介导的焦亡(图9)。研究进一步探讨了mtdsRNA的上游调控:已有研究表明氧化应激下调PNPT1表达,促进mtdsRNA释放;本研究发现牛磺酸缺乏同样可下调PNPT1并触发mtdsRNA泄漏,提示牛磺酸在维持线粒体健康中的关键作用。实验中证实mtdsRNA可同时与RIG-I和MDA5结合,其下游相互作用可能因应激条件而异。总之,mtdsRNA是IVDD进展的关键介质,靶向mtdsRNA或通过牛磺酸代谢恢复线粒体核酸稳态,可能为IVDD及下腰痛(LBP)的治疗提供新策略。
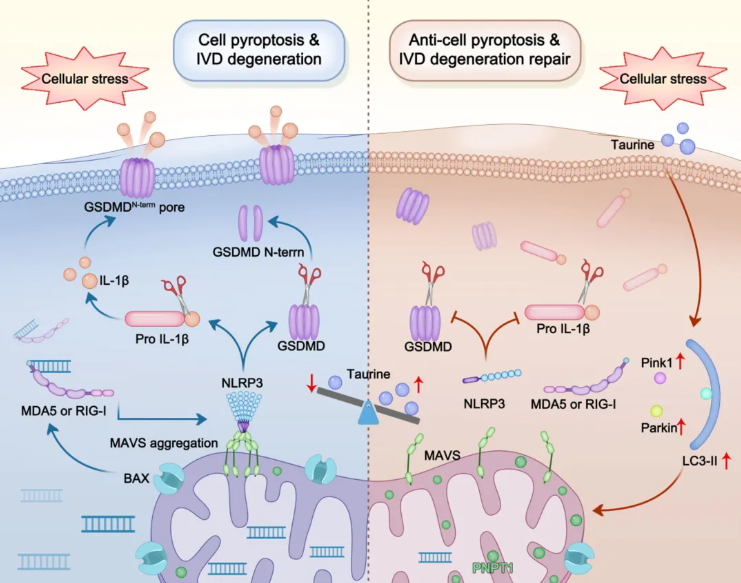
图9. 牛磺酸可以通过增强线粒体自噬来限制mtdsRNA介导的焦亡










