

文章标题:EMP1 safeguards hematopoietic stem cells by suppressing sphingolipid metabolism and alleviating endoplasmic reticulum stress
发表期刊:nature communications
影响因子:15.7
客户单位:重庆医科大学
百趣提供服务:新一代代谢组学NGM 2 Pro、定量脂质组学
研究背景
造血干细胞(Hematopoietic Stem Cells, HSCs)需维持低水平内质网(Endoplasmic Reticulum, ER)应激以保障长期自我更新与造血功能,但其调控机制尚未明确;上皮膜蛋白1(Epithelial Membrane Protein 1, EMP1)虽在白血病等血液疾病中被视为癌基因或预后因子,却未知其在正常HSCs中的作用。为探究EMP1在正常HSCs中的功能及分子机制,寻找保护HSCs免受内质网应激及电离辐射损伤的新靶点与策略,本文构建Emp1条件性敲除小鼠,结合非靶代谢组、定量脂质组、RNA-seq、ATAC-seq等组学技术,发现EMP1通过EMP1-CERS2-dhCers轴抑制鞘脂代谢、减轻ER应激以保护HSCs,为HSCs保护及相关疾病治疗提供新机制与靶点。明确EMP1保护造血干细胞的机制,为HSCs保护及辐射损伤、骨髓衰竭等相关疾病治疗提供新方向。
研究结果
01.抑制内质网应激有助于维持造血干细胞的潜能
为探究抑制内质网应激对HSCs潜能维持的影响,明确ER应激调控与HSCs功能的关联。对野生型C57BL/6J小鼠注射衣霉素(2mg/kg)诱导内质网应激,ProteoStat荧光染料检测发现骨髓HSCs的聚集蛋白水平显著升高,HSCs对衣霉素处理的未折叠蛋白反应(Unfolded Protein Response, UPR)更为显著。衣霉素组HSCs和LSK频率低于二甲基亚砜(DMSO)组,阿佐酰胺(azoramide)缓解此现象(图1B),衣霉素显著抑制了HSCs的集落形成能力,而azoramide通过抑制内质网应激,使HSCs产生的CFU数量大幅增加(图1C);另外,将经药物处理的HSCs(CD45.2)与竞争性骨髓细胞(CD45.1)共移植到致死剂量辐射小鼠体内,结果显示:azoramide或衣霉素处理分别获得了最高和最低比例的供体外周血(Peripheral Blood, PB)嵌合体(图1D-E);且在受体小鼠体内骨髓细胞、LK细胞、LSK细胞及HSCs中观察到最高和最低的嵌合体比例(图1F)。综合表明,抑制内质网应激可同时提升HSCs的体外维持能力和体内再殖能力。
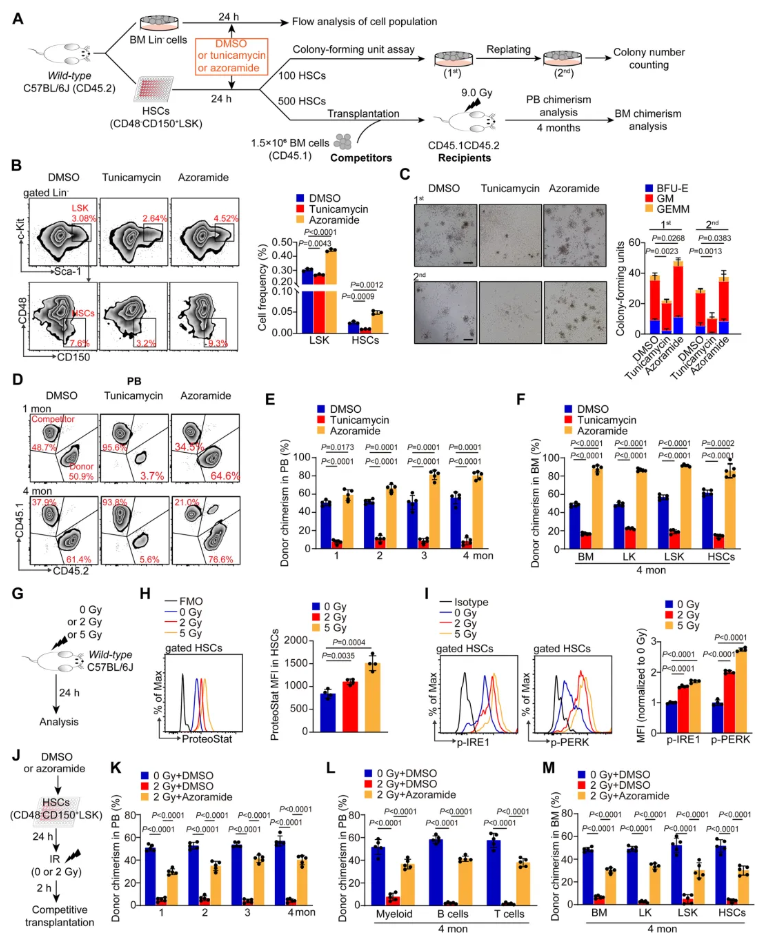
图1. 抑制内质网应激有助于体外培养及电离辐射诱导损伤下的造血干细胞(HSCs)维持
02.减轻内质网应激可保护造血干细胞免受辐射诱导的损伤
为探究减轻内质网应激是否能保护HSCs免受电离辐射(Ionizing Radiation, IR)诱导的损伤,使用亚致死量γ射线照射野生型小鼠及其HSCs(图1G)。结果显示,IR可诱导HSCs产生ER应激,体外IR处理后HSCs蛋白质聚集24h达峰且持续升高,p-IRE1、p-PERK表达显著上调,体内IR处理后骨髓LK、LSK、HSCs数量减少,蛋白质聚集水平增加(图1H),且UPR标志物p-IRE1和p-PERK升高(图1I)。使用azoramide处理HSCs后再接受IR辐射,最终移植到小鼠体内(图1J),结果显示减轻ER应激可保护HSCs免受IR损伤,azoramide处理显著提升IR损伤HSCs在受者体内的外周血、骨髓细胞、LK细胞、LSK细胞和HSCs的嵌合率,且显著增强了HSCs在受体小鼠中的重建能力(图1K-M)。这表明,内质网应激在辐射诱导的HSCs损伤中起着关键作用,而减轻内质网应激能有效改善辐射条件下HSCs的功能。
03.内质网应激诱导造血干细胞中EMP1的表达,且EMP1定位于内质网中
对衣霉素处理小鼠的HSCs进行RNA-seq和ATAC-seq测序。RNA-seq显示衣霉素诱导的内质网应激显著改变了HSCs的基因表达(图2A),基因集富集分析(GSEA)显示,内质网应激通过NF-κB通路激活了细胞凋亡、p53信号通路和TNF信号通路等特定通路(图2B)。ATAC-seq分析显示衣霉素处理的HSCs表现出整体染色质开放性显著增加(图2C-D),图2E展示了内质网应激下ATAC-seq峰位点相关基因富集的主要信号通路。将RNA-seq和ATAC-seq的数据重叠,重点关注ATAC峰与基因表达均上调的基因,其中Bcl2a1a和EMP1是上调最显著的基因之一(图2F)。单细胞RNA 测序(scRNA-seq)分析健康人骨髓细胞显示,EMP1 在HSCs中表达水平最高。qRT-PCR进一步验证,EMP1在小鼠不同造血细胞亚群中,以HSCs(CD48⁻CD150⁺LSK)的表达量最高(图2G)。为确认EMP1是否属于内质网蛋白,对小鼠骨髓细胞、人脐带血 细胞的ER组分进行WB分析,并对小鼠HSCs进行免疫荧光染色。结果显示,EMP1在HSCs中主要定位于内质网(图2H)。进一步验证显示,内质网应激(衣霉素处理)条件下,HSCs中EMP1的蛋白水平显著升高(图2I);此外,因IR可诱导HSCs产生内质网应激,IR处理也能使HSCs中EMP1的mRNA和蛋白水平显著上调(图2J-K)。综合表明:EMP1在HSCs中定位于内质网,且内质网应激可触发EMP1的表达。
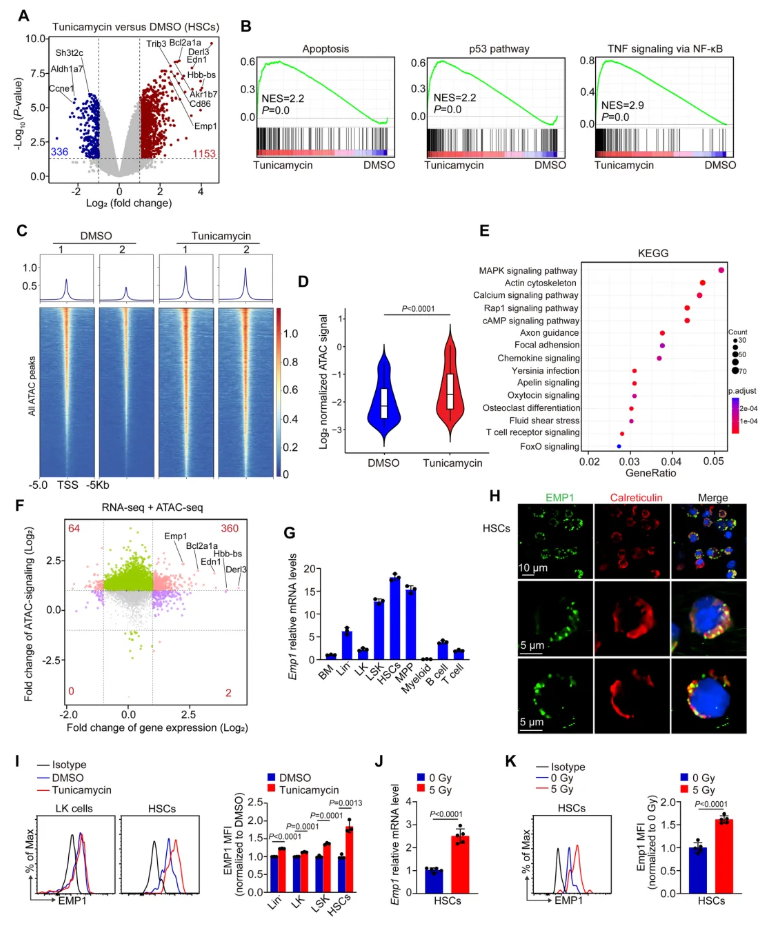
图2. 内质网应激会诱导造血干细胞中EMP1的表达,且EMP1定位于内质网中
04.Emp1缺乏会损害HSCs的维持和自我更新
为明确Emp1缺失对HSCs维持及自我更新能力的影响,探究EMP1在HSCs稳态调控中的必要性。构建Emp1条件性敲除小鼠(Emp1-cKO),WB和qRT-PCR验证了骨髓细胞与HSCs中 EMP1 的敲除效率。Emp1-cKO小鼠的骨髓细胞数量较对照组显著减少(图3A),细胞表面标志物染色显示,Emp1-cKO小鼠骨髓中的HSCs和祖细胞数量明显减少(图3B-F)。限制性稀释试验表明Emp1-cKO小鼠中功能性HSCs的频率降低(图3G)。Emp1缺失HSCs的首次及二次集落形成数均减少。为探究Emp1是否通过细胞内在机制调控HSCs的自我更新,通过竞争性连续移植实验发现PB、骨髓细胞、LK、LSK及HSCs的嵌合比例下降表明,Emp1缺失损害了HSCs的自我更新能力(图3I-L),而Emp1过表达HSCs的供体细胞在受体小鼠体内持续增加PB和BM细胞的嵌合比例。综合可知,Emp1对维持HSCs的长期自我更新至关重要。
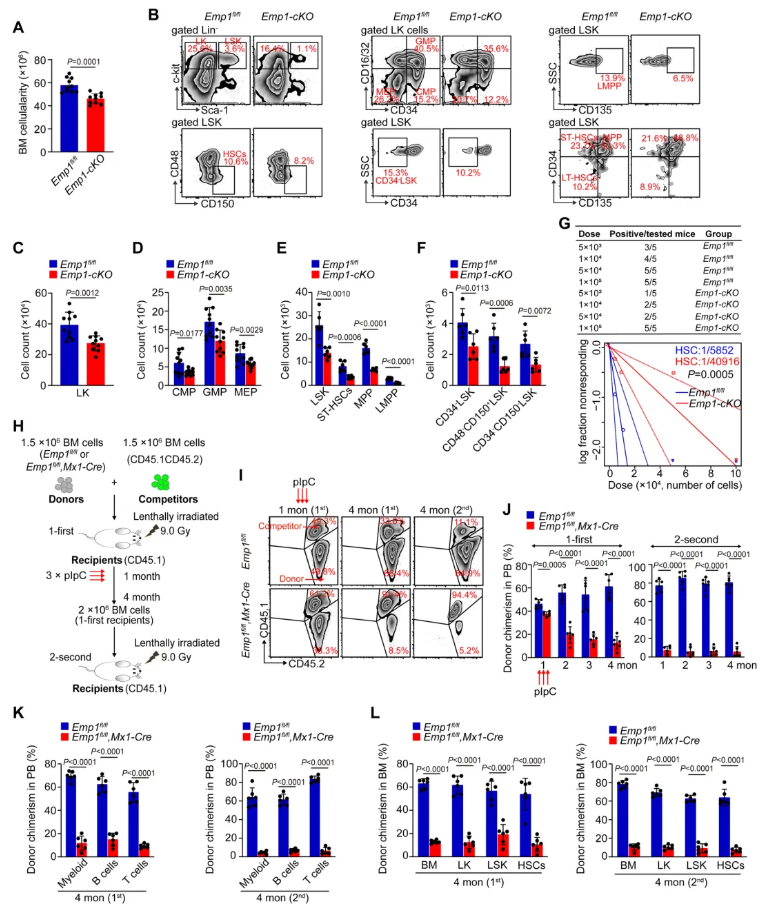
图3. Emp1缺乏会损害HSCs的维持和自我更新
05.Emp1缺乏导致HSCs中蛋白质聚集和ER应激的形成
为探究Emp1缺失是否会导致HSCs中蛋白质聚集与ER应激升高,明确EMP1在HSCs蛋白质稳态与ER应激调控中的作用。对Emp1fl/fl和Emp1-cKO小鼠的HSCs进行Ki-67+DAPI染色、Annexin-V+DAPI染色及RNA测序。结果显示Emp1-cKO小鼠HSCs的静息比例降低,早期/晚期凋亡率升高(图4A-B)。测序发现Emp1-cKO HSCs中有163个基因显著上调、316个基因显著下调(图4C),基因本体(GO)显示髓系细胞分化相关基因及造血调控基因存在显著失调(图4D),GSEA分析发现Emp1-cKO HSCs中ER应激响应相关基因显著富集(图4E)。此外,Emp1-cKO HSCs的蛋白质聚集水平显著高于对照(图4F),且GRP78、p-PERK、p-eIF2α、ATF4、p-IRE1及CHOP表达均显著上调(图4G-H);电镜显示Emp1-cKO HSCs的ER出现明显水肿与扩张(图4I)。敲低人脐血CD34+细胞中EMP1后,蛋白质聚集水平升高、凋亡率增加(图4J-K)。这表明:在小鼠造血干细胞和人类HSPCs中,EMP1基因敲除或敲低分别会导致蛋白聚集及随后引发的内质网应激反应。
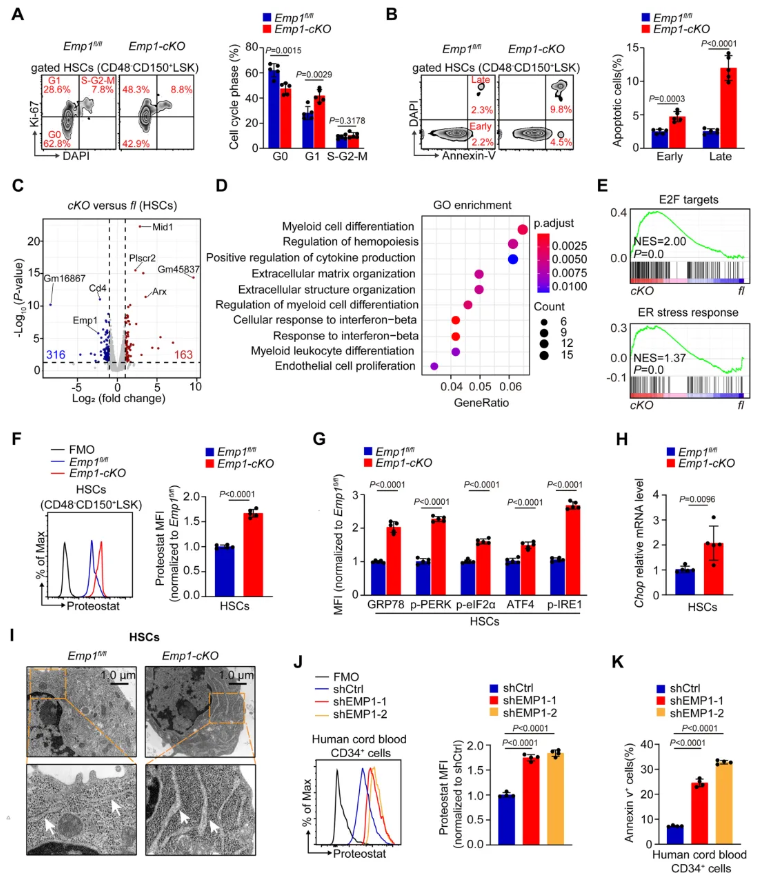
图4. 在HSCs中,Emp1缺失会导致蛋白质聚集的形成并诱导ER应激
06.Emp1缺乏导致HSCs中蛋白质聚集和ER应激的形成
为探究Emp1缺失是否会加剧HSCs在电离辐射条件下的功能缺陷,明确EMP1在HSCs抵御IR损伤中的作用。将Emp1fl/fl与Emp1-cKO小鼠暴露于不同剂量γ射线(图5A),结果显示:Emp1-cKO小鼠在IR处理后的生存时间缩短(图5B)。尤其在2Gy处理下,Emp1-cKO小鼠骨髓中LK、LSK、HSC数量较对照小鼠减少更显著(图5C–G)。同时,IR处理后,蛋白质聚集水平、p-IRE1和p-PERK表达均升高(图5H-J),凋亡率更高(图5K),静息比例降低(图5L)。综上所述,Emp1缺失会加剧电离辐射条件下造血干细胞的损伤。
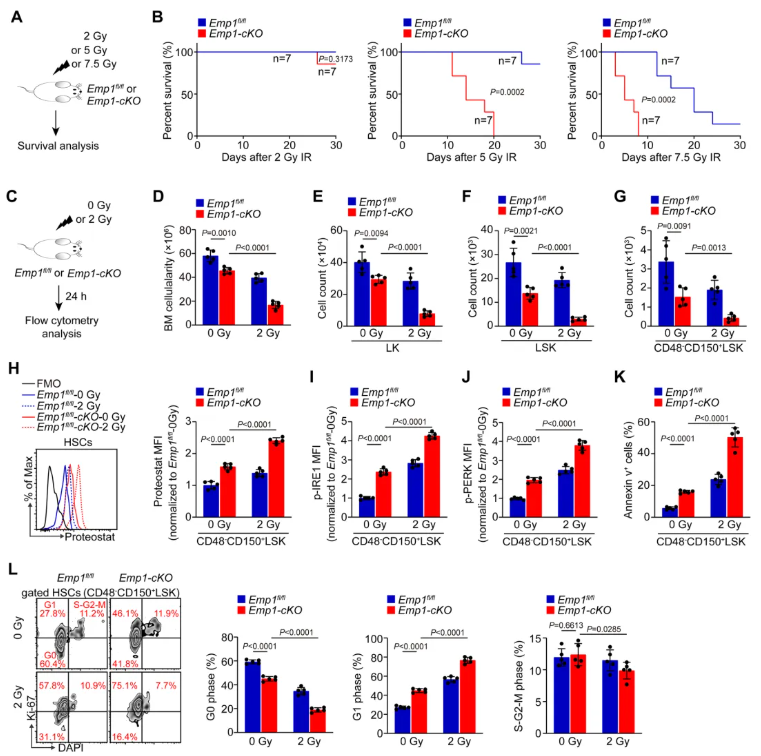
图5. 在IR条件下,Emp1的缺失会加重HSC缺陷
07.Emp1的缺失导致dhCer在HSCs中的积累
为探究Emp1缺失导致HSCs中蛋白质聚集的潜在代谢机制,明确Emp1缺失是否会引起特定脂质分子积累,以及该脂质积累对HSC功能的影响。对Emp1fl/fl与Emp1-cKO小鼠的HSCs进行非靶标代谢组学和定量脂质组学检测。非靶标代谢组学共鉴定出283种代谢物,两组间存在33种差异代谢物(图6A),KEGG富集分析显示鞘脂信号通路存在显著失调(图6B)。神经酰胺是所有复杂鞘脂(包括鞘磷脂和糖鞘脂)的核心成分(图6C)。定量脂质组学分析显示,由于Emp1缺失,造血干细胞中的二氢神经酰胺(dhCer)显著增加,尤其是dhCer(d18:0/24:1)(图6D)。向造血干细胞的培养基中添加dhCer(d18:0/24:1),并在体外和体内评估其功能(图6E),体外添加dhCer(d18:0/24:1)后,HSCs的蛋白质聚集水平显著升高(图6F),且集落形成数量显著减少(图6G);dhCer预处理的HSCs移植后,受者小鼠PB和BM中的供体嵌合率持续下降(图6H–K)。综上所述,Emp1缺失会导致造血干细胞中二氢神经酰胺的积累。此外,dhCer积累会导致蛋白质聚集体的形成,并对造血干细胞的体外和体内功能产生不利影响。
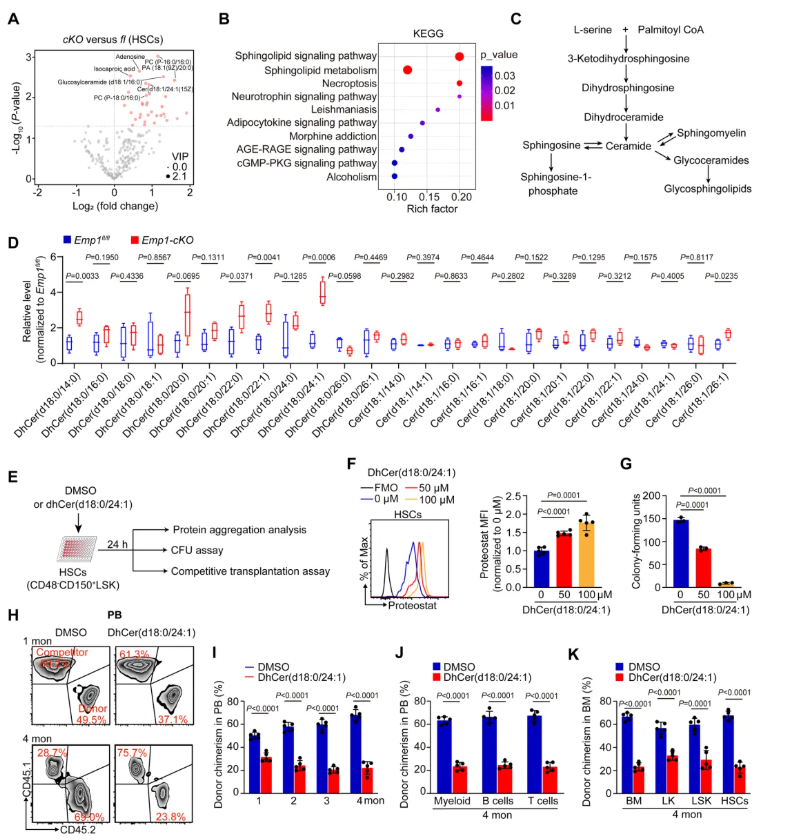
图6. Emp1缺乏导致dhCer积累,从而诱导蛋白质聚集的形成
08.EMP1结合CERS2以限制dhCer的产生
为明确EMP1限制dhCers生成的分子机制,阐明EMP1-CERS2-dhCers轴的调控关系。图7A展示了dhCer的过量生成或消耗不足过程有多种酶参与。采用IgG或HA抗体进行免疫共沉淀(co-IP)和质谱检测(图7B),分析发现EMP1与CERS2在HSCs中直接结合(图7C-E)。分子对接显示EMP1作用于CERS2的Lag1p催化结构域,该结构域突变后互作消失(图7F-H)。对Emp1-cKO小鼠注射pIpC诱导Emp1缺失后,用CERSs抑制剂伏马菌素B1(FB1)处理,发现Emp1-cKO小鼠骨髓中BM细胞、LK、LSK及HSCs数量显著恢复(图7L-O)。这表明,EMP1通过与酶CERS2相互作用来限制dhCer的积累,从而抑制内质网应激并维持HSCs的稳态。
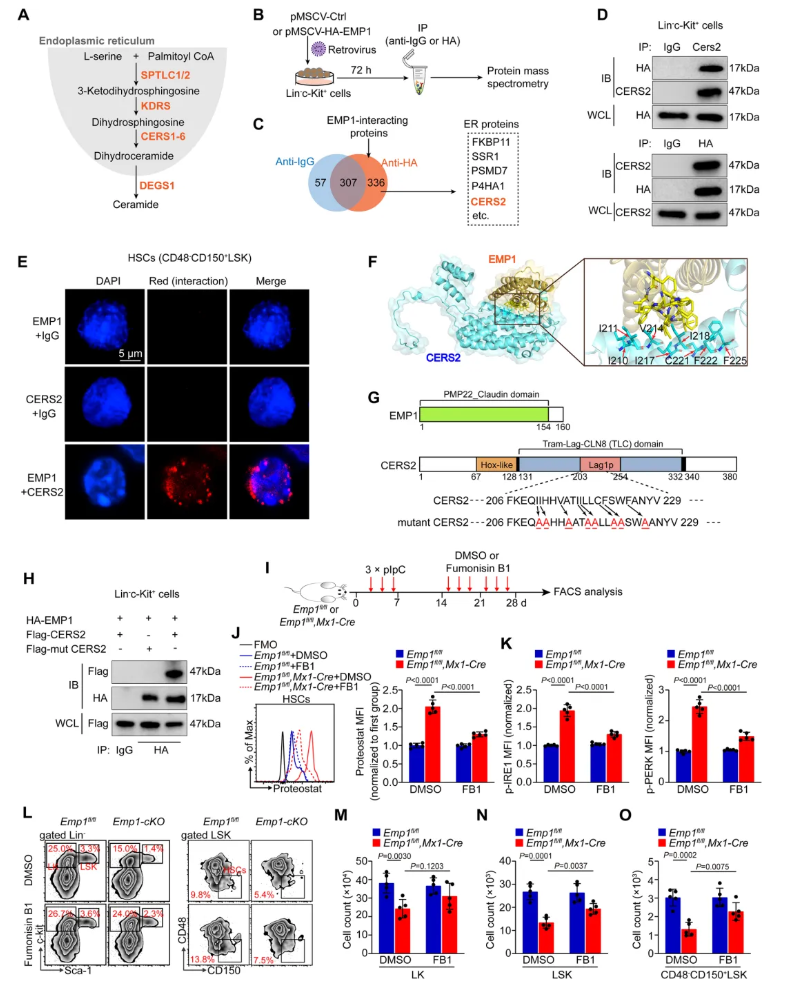
图7. EMP1结合CERS2的Lag1p结构域,以限制dhCer的产生
09.Emp1过表达或CERS2抑制保护HSCs免受IR诱导的损伤
为评估EMP1过表达或CERS2抑制是否能保护造血干细胞免受电离辐射诱导的损伤,对EMP1过表达小鼠和抑制CERS2小鼠进行IR辐射(图8A),IR处理后,EMP1过表达组供体嵌合率随时间逐渐升高(图8B),EMP1过表达显著增强了经辐射处理的造血干细胞的植入能力(图8C-D)。FB1处理显著降低IR诱导的HSCs蛋白质聚集水平(图8F),p-IRE1和p-PERK蛋白的内质网应激反应标志物水平下降(图8G);FB1处理对未受辐射处理的造血干细胞的重建能力无显著影响。但增强了经辐射处理的造血干细胞在受体小鼠中的重建能力(图8H-J)。这表明,EMP1过表达或CERS2抑制可有效保护造血干细胞免受辐射诱导的损伤。这些结果凸显了EMP1-CERS2-dhCer轴在抑制内质网应激和维持造血干细胞潜能方面的关键作用(图8K)。
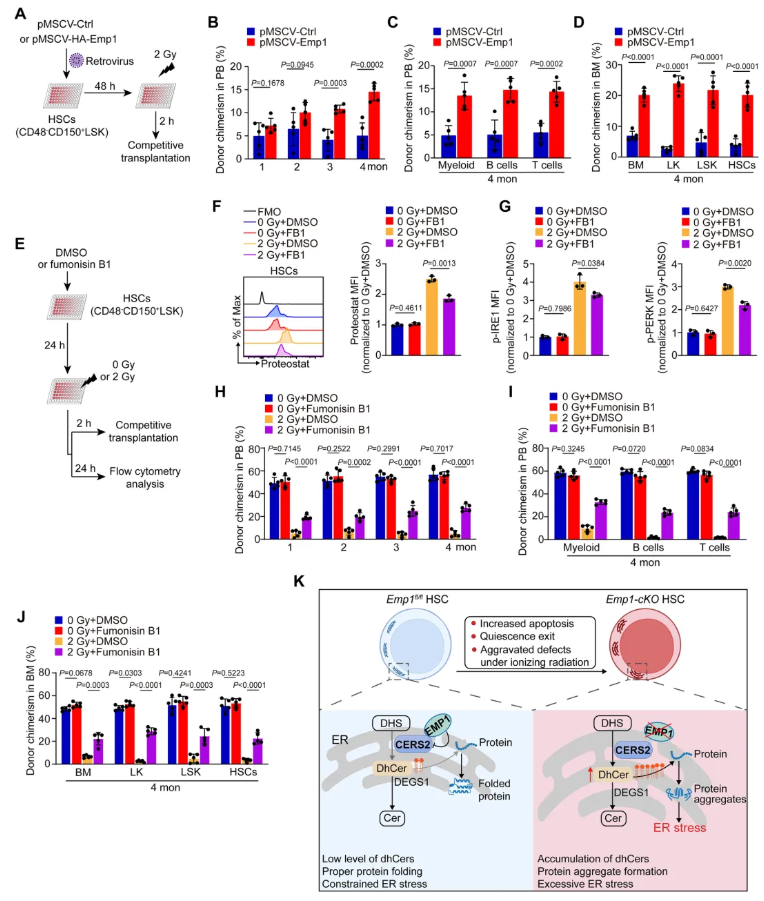
图8. Emp1过表达或CERS2抑制保护HSCs免受IR诱导损伤
研究总结
Emp1通过定位于HSCs的内质网,直接结合CERS2的Lag1p催化结构域以抑制其活性,从而限制二氢神经酰胺(尤其dhCer)的生成;Emp1缺失会导致dhCers在HSCs中积累,进而诱发蛋白质聚集与内质网应激升高,最终造成HSCs静息退出、凋亡增加、维持与自我更新能力受损,且会加剧电离辐射诱导的HSCs数量减少、应激过载与功能缺陷;而EMP1过表达或使用FB1抑制CERS2,可通过降低dhCers水平、缓解ER应激,有效保护HSCs免受IR损伤,综上证实EMP1-CERS2-dhCers轴是约束HSCs ER应激、维持其功能与抗损伤能力的关键通路,为HSCs保护及相关血液疾病干预提供新机制与靶点。










