

英文标题:Prunella vulgaris polyphenols alleviate liver injury-uveitis comorbidity by regulating acylcarnitine via the S100A9-PP2A-AMPK pathway
中文标题:夏枯草多酚通过S100A9-PP2A-AMPK通路调节酰基肉碱,缓解肝损伤与葡萄膜炎的共病
发表期刊:Phytomedicine
影响因子:8.3
合作产品:中药NGM 2
研究背景
肝损伤与葡萄膜炎作为两种严重威胁人类健康的疾病,因肝眼系统在生理与病理层面的紧密关联,临床中常出现两者共病现象,导致病情复杂化、治疗难度显著增加。然而,目前缺乏稳定模拟肝损伤与葡萄膜炎共病的动物模型,且针对其病理机制的研究仍属空白。
夏枯草(Prunella vulgaris L.)作为传统中药,以“清肝明目”功效著称,其多酚类活性成分(夏枯草多酚,PVPs)在改善肝损伤与葡萄膜炎中展现出潜力。但现有研究多聚焦单一器官治疗效应,对PVPs在肝眼共病中的双器官协同作用及其关键活性成分与作用机制的系统探索仍属空白。
本研究聚焦这一科学问题,通过构建d-GalN/LPS(D-氨基酸半乳/脂高糖)腹腔注射诱导的肝损伤-葡萄膜炎共病大鼠模型,结合代谢组学与蛋白质组学解析其病理机制,并利用酰基肉碱与S100A9抑制剂验证关键通路(S100A9-PP2A-AMPK-CPT1)的病理意义。同时,评估PVPs对共病模型的治疗效果,通过网络药理学与分子对接技术筛选PVPs关键活性成分,并以动物实验验证代表性成分对肝损伤与葡萄膜炎的改善作用,旨在为临床共病治疗药物研发提供新方向。
研究结果
1、D-GalN/LPS在大鼠中同时引发肝损伤与葡萄膜炎
在构建的D-GalN/LPS模型中,一定剂量的LPS(1 mg/kg)辅以d-GalN能够显著加重肝指数(图1A),促使血清ALT和AST均显著升高,均具有浓度依赖性(图1B)。此外,d-GalN也会加重LPS引起的炎性浸润(图1C)、葡萄膜炎典型症状(图1D)、睫状体炎性浸润(图1E)和视网膜血管扩张和血管炎(图1F),并随着剂量增加愈发严重,严重时甚至会促使细胞死亡。检测相关炎症因子,同样地,d-GalN也以剂量依赖性方式加剧了LPS刺激的炎症因子水平(图1G)。
总的来说,LPS单独处理能够引发葡萄膜炎但无显著肝损伤,而d-GalN/LPS处理显著诱导肝损伤和葡萄膜炎,且d-GalN剂量越高,症状越严重。对比不同浓度的致病效果,作者认为剂量为150 mg/kg:1 mg/kg的处理是构建肝损伤-葡萄膜炎共病模型的理想选择,可用于后续实验。
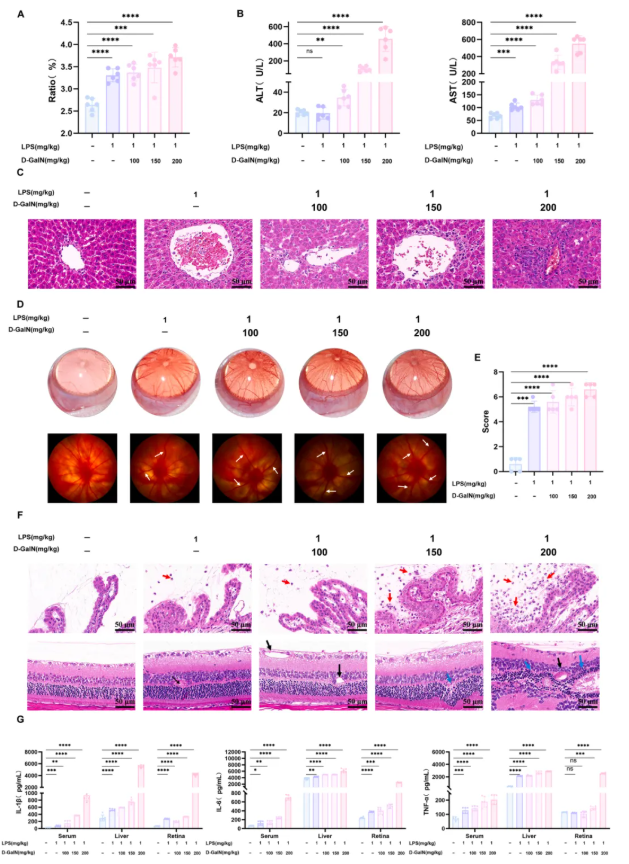
图1. D-GalN/LPS诱导的肝损伤合并葡萄膜炎在大鼠中的效应
2、酰基肉碱可能是由d-GalN/LPS引起的肝损伤-葡萄膜炎中的关键致伤因子
为挖掘肝损伤-葡萄膜炎共病的关键代谢物,作者通过代谢组学分析,发现D-GalN/LPS显著改变了大鼠肝脏和视网膜的代谢物水平(图2A)。其中,在正负离子模式下,肝脏或视网膜中代谢物变化如图2B所示。结合Venn分析,肝脏与视网膜中的63种共同代谢物被筛选(图2C),其都显著富集于脂肪酸氧化通路(图2D)。值得注意的是,在此通路下,酰基肉碱(Acylcarnitine)与多种炎症性疾病高度相关。在本研究中,大鼠肝脏中14种酰基肉碱代谢物显著增加,视网膜中5种显著增加(图2E,表1),并且总体酰基肉碱含量显著升高。由此,作者推断D-GalN/LPS诱导的大鼠肝损伤-葡萄膜炎可能与酰基肉碱的异常增加相关。
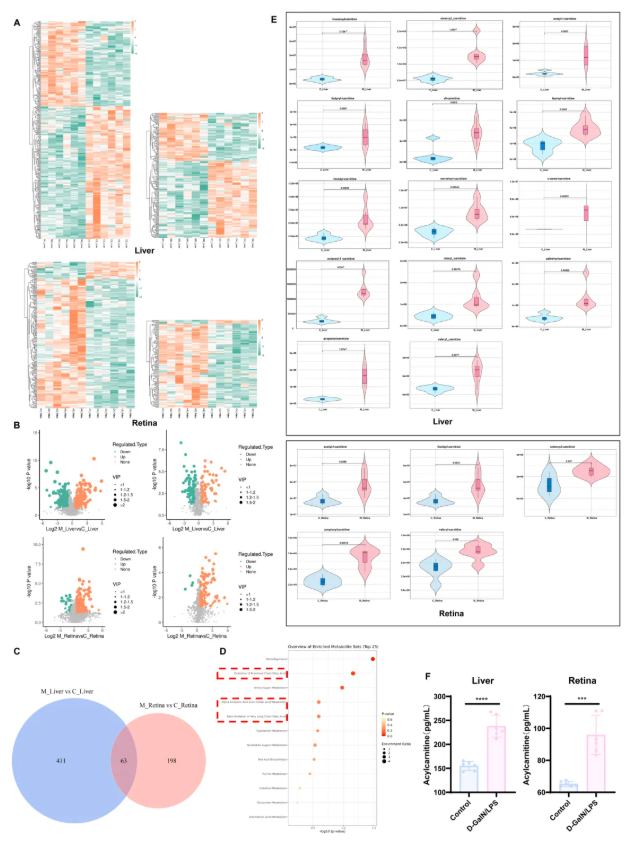
图2. 肝脏和视网膜中的代谢组学分析
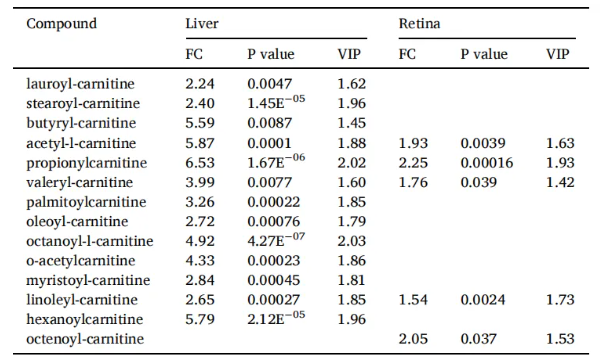
表1. 模型小鼠和对照小鼠肝脏和视网膜中酰基肉毒碱的差异
3、抑制酰基肉碱合成可缓解由d-GalN/LPS引起的肝损伤和葡萄膜炎症状
为验证酰基肉碱的关键作用,Mildronate,一种酰基肉碱合成抑制剂,被用于此次实验中。结果发现,该抑制剂不仅显著抑制了d-GalN/LPS引起的肝指数升高(图3A-B)(特别是血清ALT和AST水平),也有效防止了正常肝细胞死亡和炎性细胞浸润(图3C),表明其能够有效改善d-GalN/LPS诱导的大鼠肝损伤。
除此之外,该抑制剂也对葡萄膜炎症状(图3D)、眼评分(图3E)、睫状体炎性细胞浸润和视网膜褶皱(图3F)等方面具有积极作用,即证明了Mildronate亦可以有效改善d-GalN/LPS诱导的大鼠葡萄膜炎。
结合炎症因子水平分析,Mildronate不仅抑制了d-GalN/LPS诱导的肝脏和视网膜炎症反应(图3G-3I),而且也抑制住了酰基肉碱水平的升高(图3J)。
综上所述,酰基肉碱可能是d-GalN/LPS诱导的肝损伤-葡萄膜炎的关键因子之一。
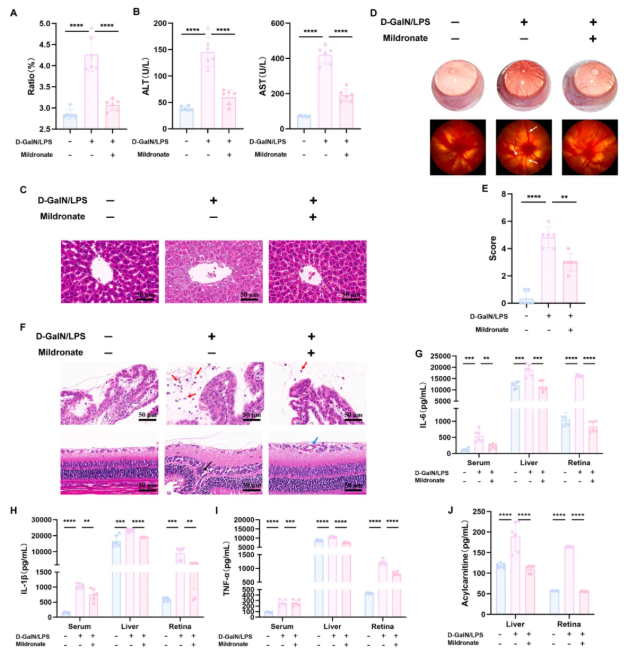
图3. Mildronate对d-GalN/LPS致肝损伤合并葡萄膜炎的治疗作用
4、S100A9可能在由d-GalN/LPS诱导的肝损伤-葡萄膜炎中起关键作用
为锚定其中作用的关键蛋白,通过蛋白质组学分析,揭示了d-GalN/LPS处理组在肝脏和视网膜中表现出的显著蛋白表达差异情况(图4A),而此些差异蛋白也高度富集于炎症和免疫反应相关通路(图4C),暗示着d-GalN/LPS可能通过激活炎症和免疫反应引发肝脏和视网膜损伤。此外,基于肝脏与视网膜的蛋白上下调情况(图4B),作者还发现与炎症和免疫密切相关的S100A9 在d-GalN/LPS处理下的大鼠肝脏和视网膜中均显著上调,而此结果也与Western blot相一致(图4D)。因此,推测S100A9可能在d-GalN/LPS诱导的大鼠肝损伤-葡萄膜炎中发挥关键作用。
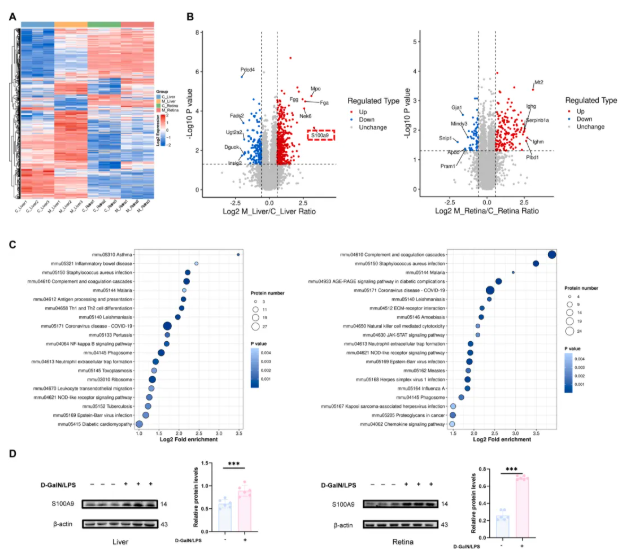
图4. 肝脏和视网膜中的蛋白质组学分析
5、抑制S100A9可缓解d-GalN/LPS诱导的肝损伤-葡萄膜炎
在给实验小鼠服用一种名为Paquinimod的S100A9抑制剂后,由dGalN/LPS所引起的肝指数(图5A)及血清ALT和AST水平(图5B)的上升均有被显著缓解;同时,注射鼠的肝细胞死亡(图5C)、视网膜血管扩张和弯曲症状(图5D)、眼症状评分(图5E)、睫状体炎症浸润(图5F)等也有好转迹象。因此,d-GalN/LPS诱导的肝损伤与葡萄膜炎与S100A9水平升高密切相关。
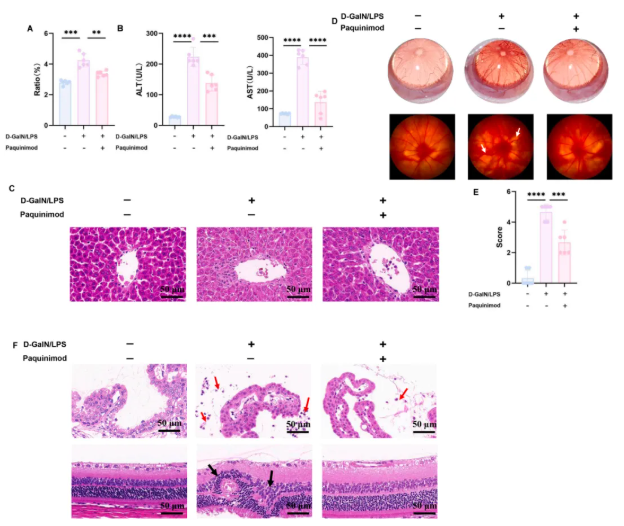
图5. Paquinimod对d-GalN/LPS诱导的肝损伤-葡萄膜炎的治疗作用
6、抑制S100A9会降低肝脏和视网膜中的PP2A活性,促进AMPK激活,上调CPT1,减少酰基肉碱含量,并抑制炎症反应
S100A9抑制剂,Paquinimod,一方面有效缓解d-GalN/LPS诱导的炎症反应(图6A);另一方面,也显著抑制d-GalN/LPS引起的肝脏和视网膜中酰基肉碱的积累。这可能暗示着Paquinimod对肝损伤和脉络膜炎的改善可能与酰基肉碱减少相关(图6B)。
肉碱棕榈酰转移酶1A(CPT1A)是酰基肉碱合成的关键酶。在d-GalN/LPS处理组中,肝脏和视网膜中S100A9的表达上调,但CPT1A下调;此时Paquinimod加入却呈相反情况(图6C),表明S100A9能够抑制了CPT1A的表达。
据现有研究报道,AMPK磷酸化与CPT1A的表达及酰基肉碱积累密切相关。作者推测并测定了大鼠肝脏和视网膜中总AMPK和磷酸化AMPK(p-AMPK)的水平,验证出S100A9通过抑制AMPK磷酸化来抑制CPT1A的表达,但不影响AMPK本身的表达(图6D)。
基于前人研究,作者推测S100A9可直接与PP2A结合,从而增强PP2A去磷酸化活性,进而抑制AMPK磷酸化。随后也发现Paquinimod显著抑制了d-GalN/LPS引起的PP2A活性升高(图6E),二者之间确有联系。
综上所述,推测d-GalN/LPS通过激活S100A9-PP2A-AMPK通路、抑制CPT1A表达并促进酰基肉碱积累,诱导肝细胞损伤和葡萄膜炎。
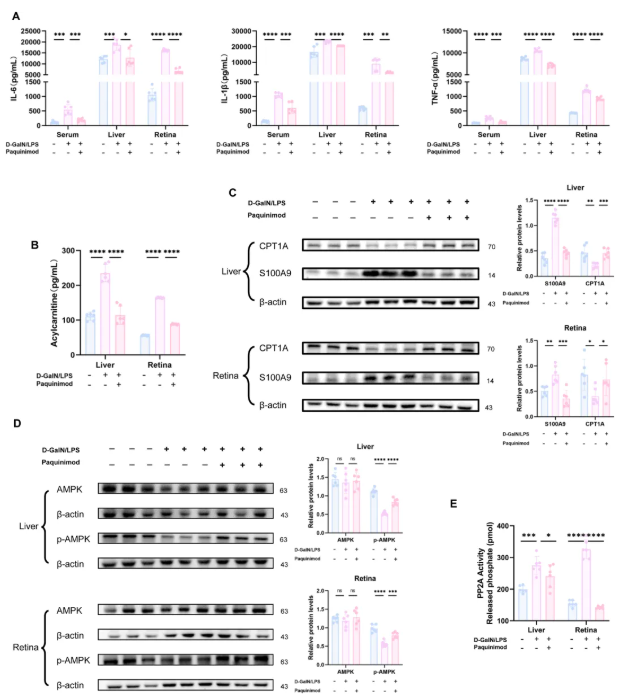
图6. Paquinimod对大鼠相关蛋白表达、酰基肉碱水平及炎症因子的影响
7、PVPs抑制肝脏和视网膜的炎症,从而缓解d-GalN/LPS诱导的肝损伤-葡萄膜炎
在大鼠中通过灌胃给予夏枯草多酚(PVPs),以研究其在缓解d-GalN/LPS诱导的肝损伤和葡萄膜炎中的作用。在肝指数方面,抗炎药DXMS加重了肝指数的升高,而PVPs却显著降低了大鼠的肝指数(图7A)。在肝功能方面,DXMS和PVPs均有效抑制了血清ALT和AST水平升高,且PVPs的效果更佳(图7B)。此外,接受DXMS或PVPs治疗的大鼠,其肝细胞死亡和炎症浸润(图7C)、眼部症状(图7D)、眼症状评分(图7E)、睫状体炎症浸润(图7F)、促炎因子水平(图7G)均得到有效改善。
综上,这些结果表明,PVPs可有效缓解d-GalN/LPS诱导的肝损伤和葡萄膜炎,展现出其作为治疗干预的潜力。
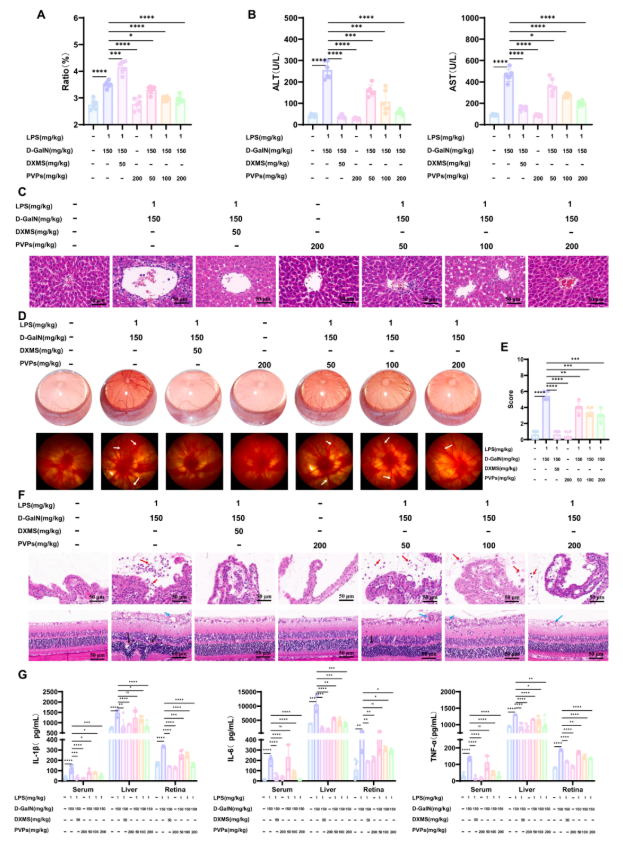
图7. PVP对d-GalN/LPS诱导的肝损伤合并葡萄膜炎的治疗作用
8、PVPs下调S100A9表达,抑制PP2A,激活AMPK,上调CPT1,并减少肝脏和视网膜中的酰基肉碱积累
基于上述结果进一步检测,发现PVPs不仅显著减少d-GalN/LPS处理大鼠肝脏和视网膜中的酰基肉碱积累(图8A),并且也能够抑制S100A9的表达、逆转了CPT1A表达的降低,其效果与Paquinimod一致(图8B)。此外,PVPs有效逆转了d-GalN/LPS诱导的p-AMPK表达减少,但未改变AMPK的总表达水平(图8C)。在PP2A活性测定中,PVPs也以剂量依赖性方式抑制了d-GalN/LPS触发的PP2A活性增加(图8D)。
综上,作者推断PVPs可有效抑制S100A9表达、降低PP2A活性、增强AMPK激活、上调CPT1A表达,并减少肝脏和视网膜中的酰基肉碱积累。通过调节这些通路,PVPs有助于改善与d-GalN/LPS诱导的葡萄膜炎相关的肝损伤。
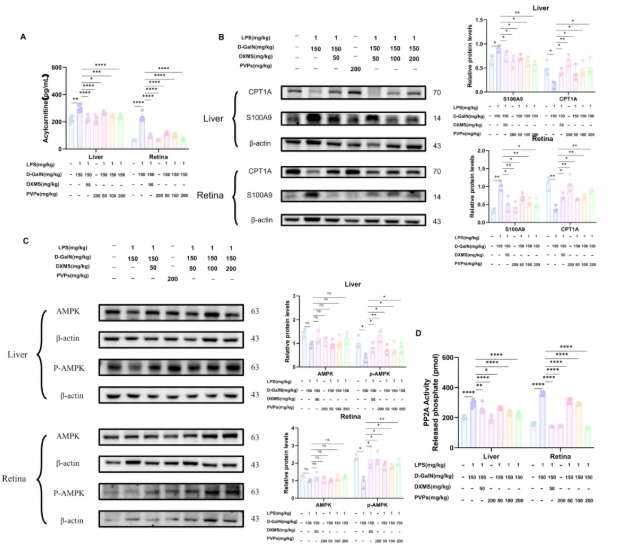
图8. PVPs对大鼠相关蛋白表达、酰基肉碱水平及炎症因子的影响
9、迷迭香酸及其相关化合物作为PVPs中治疗d-GalN/LPS诱导的肝损伤和葡萄膜炎的潜在关键活性成分
通过LC-MS/MS技术解析PVPs成分(图9A-B),共鉴定出58种化合物。结合Swiss Target Prediction数据库预测,58种成分关联总计591个靶点,其中1241个靶点与肝损伤合并葡萄膜炎相关。利用Venny软件筛选出152个重叠靶点(图9C)。基于此,构建整合58种活性成分与152个交集靶点的“活性成分-疾病-靶点”网络(图9D)。通过度值(Degree value)分析筛选出11种核心活性成分(如Salviaflaside、Rosmarinic acid等),这些成分对PVPs的保护作用具有关键贡献。
对所有58种PVPs成分与S100A9进行分子对接,发现17种成分可成功结合(图9E)。结合网络药理学预测的核心成分与分子对接结果,最终锁定6种关键活性化合物:Rosmarinic acid(迷迭香酸)、Salviaflaside、Esculetin、2-Hydroxycinnamic acid、3,4-Dihydroxybenzaldehyde和7,8-Dihydroxycoumarin。这6种成分被确认为PVPs改善肝损伤合并葡萄膜炎治疗作用的核心分子基础。
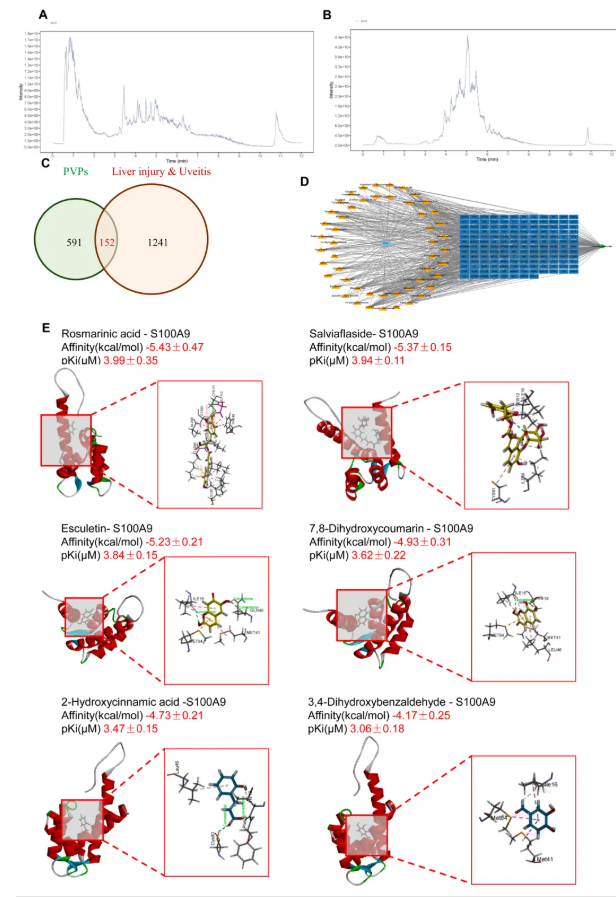
图9. 对PVPs中关键活性成分在改善肝损伤合并葡萄膜炎中的预测已被研究
10、迷迭香酸对dGalN/LPS诱导的肝损伤-葡萄膜炎的保护作用
基于分子对接结果,迷迭香酸(RosA)与S100A9的结合活性最高,确立其为自愈的关键质量控制标志物。为进一步验证PVPs中缓解d-GalN/LPS诱导的肝损伤和葡萄膜炎的主要活性成分,随后对RosA的疗效进行综合评估。结果显示,RosA显著缓解了d-GalN/LPS导致的大鼠肝指数(图10A)及ALT和AST的升高(图10B),并减轻了炎症浸润(图10C)、虹膜充血、瞳孔收缩、视网膜血管扩张和弯曲等症状(图10D),也缓解了眼部症状严重程度(图10E)、睫状体的炎症浸润和视网膜皱褶(图10F)等。
综上,迷迭香酸在改善d-GalN/LPS诱导的肝损伤和葡萄膜炎症状方面表现出显著疗效。
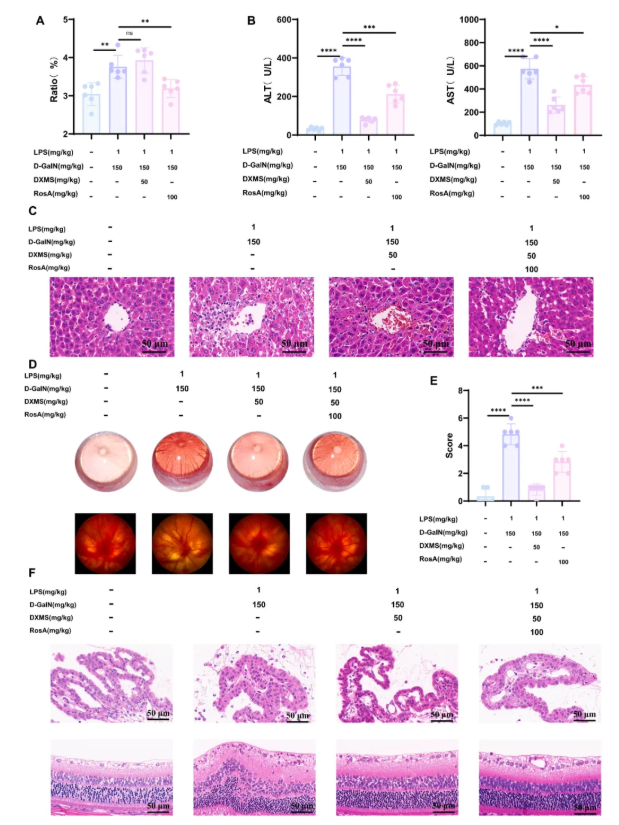
图10. RosA对d-GalN/LPS诱导的肝损伤合并葡萄膜炎的治疗作用
研究小结
本研究通过建立肝损伤与葡萄膜炎共病的大鼠模型,借由代谢组学与蛋白质组学揭示其病理机制,发现d-GalN/LPS通过激活S100A9-PP2A-AMPK通路,导致酰基肉碱积累与炎症反应;PVPs通过抑制S100A9、降低PP2A活性、激活AMPK并上调CPT1A,显著缓解肝与视网膜损伤。结合网络药理学与分子对接,筛选出迷迭香酸等6种关键活性成分,其中迷迭香酸在动物实验中验证可显著改善肝损伤(降低ALT/AST、减轻肝组织炎症)及葡萄膜炎(缓解虹膜充血、视网膜炎症)。研究为肝损伤-葡萄膜炎共病的治疗提供了新靶点,并推动PVPs在清肝明目中药的临床转化与药物开发。
中药NGM 2:依托新一代代谢组学技术,聚焦中药成分准确鉴定核心需求。联合两大专业数据库,物质鉴定标准对齐国际顶级期刊(MSI),level 1鉴定准确率高达98%,检出物质数量500+。支持中药材、血清等多类样本,助力中药机制研究!









